Alain Bouquet - Radioactivité: les Curie
Attention: ces pages ne sont plus mises à jour car le site a déménagé. Il se trouve désormais à: Pensez à mettre à jour vos signets et bookmarks! |
Champs, Noyaux & particules
Radioactivité
Noyaux, protons et neutrons
- Noyau atomique: Rutherford
- Noyau atomique: Bohr, Soddy et Moseley
- Noyau atomique: Aston et Rutherford
- Neutron: Chadwick
- Neutron: Joliot-Curie
- Neutron: Fermi
Intruments, accélérateurs et détecteurs
Mécanique quantique
- Mécanique ondulatoire
- Formalisme quantique
- Applications
- Théorie quantique des champs
- Électrodynamique quantique
Fission nucléaire
Fusion nucléaire
Particules en tout genre
Les Curie
Pierre Curie (1859-1906)
 |
S’il n’avait pas le prestige social d’un Becquerel, Pierre Curie était un physicien exceptionnel. Il avait découvert en 1880 avec son frère Jacques la piézo-électricité (la propriété du quartz de générer par déformation des charges électriques) et en avait donné l’explication, il avait étudié en détail le magnétisme (la «loi de Curie» et le «point de Curie» en gardent la mémoire), et beaucoup réfléchi aux questions de symétrie («principe de Curie»). Brillant théoricien, il était aussi un remarquable concepteur d’instruments de précision (balance de Curie, électromètre de Curie, etc.). Il fut nommé en 1882 professeur à l’École de physique et de chimie industrielles de la ville de Paris (EPCI) où il disposait d’un très modeste laboratoire. Autodidacte (son frère Jacques lui apprit beaucoup), la voie royale de la Sorbonne et de l'Académie des Sciences lui était en effet d’emblée fermée. Il dut attendre de recevoir en 1903 le prix Nobel de physique pour que la Sorbonne lui ouvre ses portes et daigne le nommer professeur en 1904, puis que l'Académie des Sciences le juge digne en 1905 d'entrer dans ses rangs. |

Pierre et Jacques Curie et leurs parents
La piézoélectricité
En 1880, Pierre Curie découvrit la piézoélectricité avec son frère Jacques: certains cristaux, dont le quartz, font apparaître des charges électriques en surface quand ils sont soumis à une pression.
 Effet piézoélectrique (Wikipedia)
Effet piézoélectrique (Wikipedia)
Il en donna aussitôt l'explication: une pression sur un cristal de quartz déplace les charges électriques:

ce qui engendre un champ électrique, d'où apparition de charges en surface, et un courant si le circuit est refermé. Inversement, appliquer un courant, donc un champ électrique, engendre une pression. Si le courant est un courant alternatif, l'alternance de compressions et de dilatations du quartz est une vibration du quartz (qui peut devenir importante si la fréquence correspond à une fréquence de résonance du cristal).

Carnet de notes de Pierre Curie: la piézoélectricité.


Balance à quartz de Pierre Curie: le quartz sert de capteur de pression (ou ici de tension)
Les usages de la piézoélectricité sont très divers, de l'allume-gaz à la montre à quartz. Le quartz (ou aujourd'hui certaines céramiques PZT qui ont la même propriété de piézoélectricité mais des qualités mécaniques supérieures) sert très souvent à convertir une pression mécanique en tension électrique (qui peut ensuite alimenter un circuit électronique, un affichage, etc.), ou inversement à permettre à un signal électrique d'actionner une commande mécanique (usage fréquents en micro-mécanique de nos jours). Cela permet des réaliser des microphones ou des hauts-parleurs de petite taille (dans les téléphones par exemple), des sonars ou des capteurs pour l'échographie ultrasonore, des capteurs de pression pour les pneumatiques, des accéléromètres (console de jeu Wii par exemple). La iste des applications est immense.

Principe d'une montre à quartz (A est une pile, le quartz est en B, C est un circuit intégré et D le micro-moteur qui fait avancer les aiguilles pas à pas)
Magnétisme
Pour son travail de thèse, Pierre Curie se tourna vers le magnétisme, et plus précisément sur les effets de la température sur l'aimantation. Il démontra que l'aimantation du fer (et plus généralement des matériaux ferromagnétiques) disparaissait au-dessus d'une température critique, appelée désormais "température de Curie" ou "point de Curie". Pour le fer, elle est de 1043 K.

Développer les bases du magnétisme (différence ferro/paramagnétique, origine de la température critique, aimantation spontanée, théorie de Langevin, etc.). Sa thèse de doctorat « Sur les propriétés magnétiques des corps à diverses températures » établit les lois applicables aux trois types d’éléments connus, diamagnétiques, paramagnétiques et ferromagnétiques et la disparition à haute température (point de Curie) des propriétés particulières de ces derniers.
Faire une section sur les principes de symétrie et l'apport de Pierre Curie. Ne pas oublier l'âne de Buridan (cf expo au Panthéon). Le principe de symétrie de Curie énonce un certain nombre de relations entre les éléments de symétrie des causes et ceux des effets produits lors d’un phénomène physique.
Instrumentation
Pierre Curie améliora fortement en 1885 la sensibilité de l'électromètre à quadrants inventé par Lord Kelvin

Schéma de Pierre Curie pour un électromètre à quadrants

Base d'un électromètre à quadrants, laissant apparaître au centre en bas le miroir suspendu au fil et permettant d'en mesurer la rotation lors du passage d'un courant électrique.
Maria Skłodowska Curie (1867-1934)
 |
La personnalité et la vie de Maria Skłodowska sont bien connues par les très nombreuses biographies de Madame Curie, à commencer par celle de sa fille Ève. Cinquième enfant du professeur Skłodowski, Maria devint, après son baccalauréat à 16 ans, préceptrice dans la famille Zorawski, pour aider sa sœur Bronia à faire ses études de médecine à Paris. Elle l’y rejoignit en 1891 quand Bronia s'installa comme médecin Elle s'inscrivit à la Sorbonne, réussissant brillament sa licence de physique en 1893, puis de mathématiques en 1894. Elle obtint alors une bourse de l'industrie métallurgique pour l’étudier les propriétés magnétiques des métaux. Elle fut donc naturellement mise en contact avec un bon spécialiste du sujet: Pierre Curie. Pierre et Marie se marièrent en 1895, puis Marie prépara l'agrégation de physique dont elle sortit première en 1896. Sa première fille, Irène, naquit le 12 septembre 1897. La seconde, Eve, ne vit le jour que le 6 décembre 1904 car Marie avait entretemps décidé de se lancer dans une thèse de doctorat ès sciences. Elle fut la première femme en France à se lancer dans cette aventure. Pierre suggéra à Marie fin 1897 de reprendre l’étude des rayons «uraniques» abandonnée par Becquerel. Elle soutint le 25 juin 1903 sa thèse «Recherches sur les substances radio-actives». Entretemps, elle avait découvert avec Pierre le polonium et le radium. Et ils reçurent ensemble le prix Nobel de physique de 1903 pour ces travaux. |

Maria, Bronisława et Helena autour de leur père

Pierre et Marie Curie partant en voyage de noces

Pierre Curie (1859-1906), physicien et Marie Curie (1867-1934), chimiste
La radio-activité
Marie reprit donc l'étude des rayons uraniques là où Becquerel venait de l'abandonne. Elle décida de rechercher si d’autres corps que l’uranium pouvaient en émettre. Becquerel avait exclu cette éventualité, mais Marie savait pouvoir disposer d'une instrumentation beaucoup plus sensible que Becquerel gâce aux instruments de Pierre. «La question était entièrement nouvelle» écrivit-elle en 1923 dans sa biographie de Pierre. Ce n’était pas tout à fait exact, d’autres physiciens avaient déjà eu la même idée, mais leurs résultats étaient très confus. Marie décida d’utiliser l’ionisation de l’air pour détecter et comparer l’activité de différents échantillons et surtout d’employer pour cela l’électromètre de Kelvin, grandement perfectionné par Pierre, pour mesurer l’intensité du courant d’ionisation de ses échantillons. La plaque photographique était lente, l’électroscope peu précis, l’électromètre était l’outil idéal, mais son utilisation était très délicate.
L’idée de base est simple : un échantillon est placé entre les deux plaques d’un condensateur (une chambre d’ionisation) dont on mesure le courant de décharge grâce à l’électromètre : le passage du courant fait pivoter un miroir suspendu à un long fil de torsion en quartz, ce pivotement dévie un faisceau lumineux réfléchi par le miroir et qui revient sur une règle graduée. La vitesse de déplacement de la tache de lumière mesure l’intensité du courant. Becquerel avait signalé que le rayonnement de l’uranium rendait l’air conducteur (il ionisait l’air). D’où l’idée de Pierre Curie de mesurer l’intensité du rayonnement via l’intensité du courant traversant une chambre d’ionisation. Montage très délicat, mais très sensible grâce à l’électromètre à quadrants inventé en 1872 par Kelvin et amélioré par Pierre.
 Chambre d'ionisation
Chambre d'ionisation
 Électromètre de Piere Curie
Électromètre de Piere Curie
 Rotation de l'électromètre
Rotation de l'électromètre
Raffinement de Pierre Curie: méthode différentielle. On ajoute une balance à quartz sur laquelle on pose un poids, qui génère une charge électrique Q. On chronomètre le temps t nécessaire au courant de la chambre d’ionisation pour équilibrer la charge Q → i = Q/t. En pratique, c’est très fastidieux ! La méthode fut néanmoins utilisée jusque dans les années 1950 avant d'être définitivement remplacée par des compteurs (Geiger par exemple).

Le « montage Curie » de mesure de la radioactivité (exposé au musée Curie à Paris) : à gauche la « boîte » est la chambre d’ionisation où est placé l’échantillon dont on mesure l’activité, au centre (au fond) l’électromètre, au premier plan, la réglette graduée et, accrochée dessous la lampe dont la lumière est réfléchie par le miroir suspendu au fil de l’électromètre. À droite, au fond, la balance à quartz ajoutée ensuite, et sa boîte de poids.
L'EPCI où Pierre était professeur était un établissement d'enseignement, formant des ingénieurs, mais pas un centre de recherche et ne disposait pas vraiment de laboratoires. Le directeur de l'école permit à Pierre (et Marie dont le statut était incertain) l'usage de hangars désaffectés.

Extérieur des hangars

Intérieur du hangar consacré à la physique

Intérieur du hangar consacré à la chimie
Une bizarrerie de la pechblende
Les carnets de laboratoire remplis - à deux mains -par Marie et Pierre Curie permettent de suivre leur cheminement, leurs hésitations, leurs doutes et leurs joies. Marie commença à utiliser l’électromètre le 16 décembre 1897, et elle ajouta au montage la balance à quartz piézo-électrique le 20 janvier pour que les mesures soient plus stables et plus précises. Sous la tension d’un poids, le quartz générait une charge électrique bien déterminée, et il ne restait qu’à mesurer avec un chronomètre le temps nécessaire au courant d’ionisation pour compenser cette charge. Ce «montage Curie» fut la clé de la réussite. Il resta utilisé plus d’un demi-siècle pour les mesures fines de radioactivité.

Marie Curie aux commandes, la main droite soulevant le poids de la balance à quartz, la main gauche tenant le chronomètre et l’œil fixé sur la tache de lumière sur la règle. À ses côtés, Pierre Curie et son assistant, Petit. L’électromètre est ici en dehors de l’image, sur la gauche. ©ACJC
Le 10 février Marie put commencer ses premières mesures, en commençant, bien entendu, par reproduire les expériences de Becquerel, et surtout de Kelvin et ses collaborateurs, sur divers échantillons de sels d’uranium. Tous les composés de l’uranium se révélèrent actifs et cela d’autant plus qu’ils contenaient plus d’uranium : l’activité était bien liée aux atomes, indépendamment de leur composition chimique. Cependant, elle remarqua le 17 février une anomalie avec deux minerais : la pechblende et la chalcolite (aujourd'hui appelée plutôt torbernite). Ils étaient deux fois plus actifs que l’uranium, et c’est là que l’on voit l’importance des mesures quantitatives précises que Marie Curie était seule à exécuter. Mais la chalcolite de synthèse ne possédait pas cette propriété, et Marie supposa donc qu’elle était due à une «impureté» contenue dans la chalcolite et la pechblende naturelles dont la composition est complexe. Elle ne s’attarda cependant pas sur cette anomalie et continua à étudier systématiquement d’autres substances.

L’anomalie notée par Marie Curie, qui conduisit à la découverte du polonium et du radium (comptes-rendus à l’Académie des Sciences, 12 avril 1898)

Pechblende

Chalcolite (ou torbernite)
Marie Curie découvrit ensuite, le 24 février 1898, que le thorium (Z=90) émettait des rayonnements ionisants similaires à ceux de l’uranium (Z=92). Elle inventa à cette occasion le terme de radioactivité, puisque le terme de "rayons uraniques" n'était plus pertinent. Cependant en Allemagne, à Erlangen, Gerhardt Schmidt l’avait précédée et il avait annoncé dès le 14 février que le thorium émettait des "rayons de Becquerel". Grâce aux relations de Pierre parmi les minéralogistes, elle put examiner «un grand nombre de métaux, sels, oxydes et minéraux» dans les collections de minéralogie de l’EPCI, de la Sorbonne et du Muséum. Mais seuls les composés de l’uranium et du thorium montrèrent une activité mesurable. Elle publia le 12 avril 1898 une note sur les «Rayons émis par les composés de l’uranium et du thorium» mentionnant l’activité anormale des minerais d’uranium. Elle se posa bien sûr la question de la source d’énergie de ces rayons, et comme le thorium et l’uranium étaient les éléments les plus lourds connus (avec des masses atomiques de 234 et 238), cela lui suggéra une explication ingénieuse:

On découvrait presque chaque année de nouveaux rayonnements et il était logique de penser que certains corps pouvaient avoir la possibilité de capter ces rayonnements traversant l’espace comme de petites antennes, plus ou moins efficaces selon la nature des corps et des rayonnements.
Ce premier article de Marie Curie contient déjà en filigrane tous les travaux suivants de Pierre et Marie Curie:
- l'activité augmente avec la quantité de l'élément responsable (elle ne parle pas de proportionnalité car elle n'était pas du tout évidente à ce moment, en raison de l'absorption par l'élément lui-même d'une partie de son activité, les alphas essentiellement)
- l'activité est une propriété atomique de l'élément, dientique quelle que soit sa forme physique ou chimique
- l'activité n'est pas propre à l'uranium (exemple du thorium), et elle devrait permette de diagnostiquer la présence de nouvelles substances
Polonium
Marie Curie regrettait cependant d'avoir été devancée par Schmidt sur le thorium et, abandonnant cet élément, elle se focalisa sur l’anomalie découverte dans la pechblende. Comme elle venait de montrer qu’aucun élément connu ne pouvait en être responsable, elle pensa qu’il devait exister dans la pechblende un élément inconnu et beaucoup plus actif que l’uranium : puisqu’il n’avait pas été décelé chimiquement jusque-là, il devait être présent à l’état de traces, et donc être particulièrement actif. Pierre la rejoignit alors dans ses recherches, et ils se lancèrent dès le 14 avril dans la séparation chimique des constituants d’un échantillon de quelques centaines de grammes de pechblende. Marie avait reçu une bonne formation de chimiste en Pologne, mais ils n’avaient bien sûr aucune idée des propriétés chimiques de ce nouvel élément, et ils tâtonnèrent donc quelque peu. Ils reçurent l’aide de chimistes de l’EPCI, Gustave Bémont en particulier, et ils utilisèrent les méthodes usuelles de chimie minérale, en se guidant « par le contrôle de l’activité radiante des produits séparés à chaque opération ». Finalement, le « corps actif » resta avec le bismuth, et ils l’en séparèrent en répétant des cristallisations fractionnées (les premiers cristaux qui apparaissaient étaient plus actifs que la solution). Ils obtinrent ainsi un corps 400 fois plus actif que l’uranium, qu’ils proposaient d’appeler polonium, en l’honneur de la patrie de Marie (alors partagée entre les empires russe, allemand et austro-hongrois). Les Curie annoncèrent leur résultat dans une note du 13 juillet 1898 à l’Académie des Sciences avec le titre « Sur une substance nouvelle radio-active, contenue dans la pechblende ». C’était la première fois qu’apparaissait publiquement le terme de radioactivité. Comme le thorium et le polonium émettaient des rayons « uraniques », ce terme ne paraissait plus approprié : il s’agissait manifestement d’une propriété nouvelle de la matière, la radioactivité.
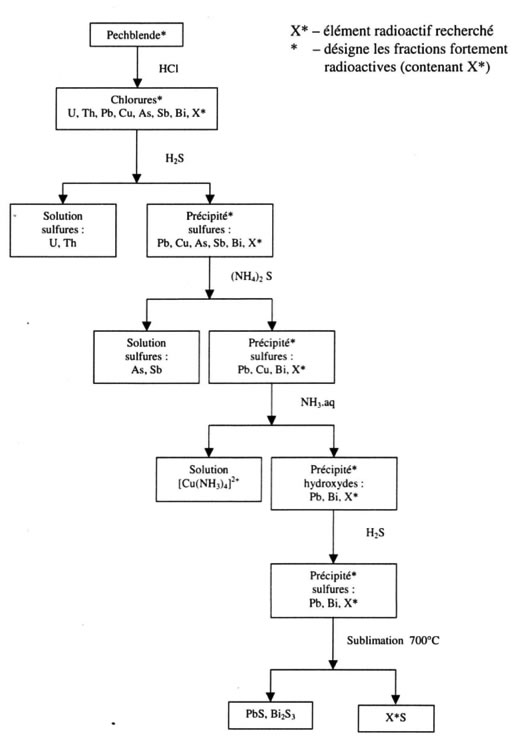
La recette du polonium © K. Kabzinska
Avec le recul, nous savons que cette substance « 400 fois plus active que l’uranium » contenait extrêmement peu de polonium : le polonium 210 est dix milliards de fois plus radioactif que l’uranium 238. Les Curie avaient en réalité isolé du sulfure de bismuth avec des traces (moins d’une partie par million) de polonium. Cela explique que la spectroscopie n’ait pu déceler d’autres raies que celles du soufre et du bismuth. Isoler le polonium fut un long travail, le laboratoire Curie ne parvenant qu’en 1910 à isoler quelques milligrammes d’une substance contenant 1% de polonium, permettant d’identifier des raies caractéristiques dans son spectre. De plus, le polonium 210 a une période de 140 jours, il disparaît donc rapidement des échantillons. Dans la nature il est constamment régénéré par les désintégrations radioactives à partir de l’uranium. Les Curie avaient en réalité isolé du sulfure de bismuth avec des traces de polonium (moins d’une partie par million). Le Po210 est 10 milliards de fois plus radioactif que l’uranium. Le célèbre « hangar » où se faisait la mesure de radioactivité à chaque étape de la séparation du polonium.
Radium
En isolant le polonium, les Curie avaient repéré la présence d’une autre substance radioactive, plus rare et au comportement chimique complètement différent et analogue à celui du baryum. Après une pause de trois mois, sans doute pour attendre la livraison de 5 kilos de pechblende, les travaux reprirent le 11 novembre. La méthode de séparation était analogue, quoique différant dans les détails, et Gustave Bémont apporta à nouveau une aide précieuse aux Curie. La nouvelle substance était si voisine du baryum qu’il était, là encore, impossible de l’en séparer par des méthodes purement chimiques et il fallut à nouveau recourir à la cristallisation fractionnée. La nouvelle substance demeurait mêlée à une forte proportion de baryum, mais l’activité du mélange dépassait 900 fois celle de l’uranium, et une raie inconnue apparaissait dans son spectre. Sur ces bases, les Curie proposèrent, le 26 décembre 1898, dans une communication à l’Académie des Sciences l’existence d’une nouvelle substance extrêmement radioactive, à laquelle ils donnèrent le nom de radium.


Ici encore, les Curie avaient en réalité isolé du sulfure de baryum contenant moins de 0,1% de radium, qui est 3 millions de fois plus radioactif que l’uranium. Il était cependant clair pour les Curie que des quantités énormes de minerai, se chiffrant en tonnes, seraient nécessaires pour extraire des quantités utiles de radium : pour continuer les recherches, il fallait passer rapidement à une échelle industrielle ! En 1902, Marie parvient à isoler 0,1 g de chlorure de radium, lui permettant d’estimer à 225±1 sa masse atomique.
Pourquoi trouve-t-on du radium et du polonium dans les minerais d'uranium? La réponse vint quelques années plus tard, quand Rutherford et ses collaborateurs établirent que la radioactivité était la conséquence de transmutations dans lesquelles un atome (en fait un noyau) se transforme en un autre, que ce phénomène pouvait se répéter et donc conduire à des chaînes de transmutation radioactives aux étapes nombreuses. Quand les physiciens finirent par démêler l'écheveau de ces transmutations, en introduisant en particulier la notion d'isotope (due à Soddy), il s'avéra que la séquence des transmutationsà partir de l'uranium, qui est à l'état natuel à 99.3% de l'uranium 238, est la suivante:


À un instant donné, toutes les étapes de la chaîne sont simultanément présentes (en quantité extrêmement variable dépendant de leur demi-vie radioactive). Dans un minerai d'uranium, on trouve donc inévitablement du radium 226 et du polonium 210.
Radioexcitation

La découverte du radium eut un retentissement aussi grand que celle des rayons X deux ans plus tôt. La personnalité des découvreurs y était pour beaucoup, mais aussi la radioactivité considérable du radium. La découverte du radium ressuscita l’intérêt pour les rayons de l’uranium et du thorium. Ernest Rutherford à Cambridge, puis à Montréal, André Debierne et Paul Villard à Paris, Friedrich Oskar Giesel, Stefan Meyer et Egon von Schweidler à Vienne, Julius Elster et Hans Friedrich Geitel à Heidelberg, Friedrich Ernest Dorn à Halle, William Ramsay à Londres, tous se passionnèrent pour la radioactivité. Même Becquerel s’y remit ! Le prix Nobel de physique le récompensa en 1903 pour sa découverte de la radioactivité, ainsi que Pierre et Marie Curie pour leurs contributions à l’étude de cette radioactivité. Pierre dut beaucoup insister pour que Marie partage le prix avec lui, et le prix ne mentionnait pas le polonium, ni le radium, dont l’existence était alors contestée par les chimistes (ce n’est qu’après avoir isolé du radium sous forme métallique que Marie Curie reçut le prix Nobel de chimie en 1911).

Caricature parue en 1904 dans Vanity Fair ©ACJC
Rutherford avait montré dès janvier 1899 que le rayonnement de l’uranium était de deux types, qu’il baptisa alpha et bêta : les rayons alpha ionisaient fortement l’air mais étaient peu pénétrants, les rayons bêta ionisaient moins mais pénétraient plus les obstacles. Les Curie retrouvèrent cette même distinction pour le rayonnement du radium en novembre 1899. Dans leur laboratoire, toujours en 1899, Debierne découvrit dans la pechblende un nouveau corps radioactif, l’actinium. La même année, Becquerel identifia les rayons bêta aux rayons cathodiques (les électrons) et, en même temps que Giesel, il montra qu’ils étaient déviés par un champ magnétique. En avril 1900, Villard observa un troisième type de rayonnement, bien plus pénétrant que les deux autres et non dévié par un champ magnétique, les rayons gamma. Max von Laue montra en 1912 qu’il s’agissait d’un rayonnement électromagnétique, comme la lumière ou les rayons X, mais de plus courte longueur d’onde. Les rayons alpha semblaient plus intéressants pour la physique du fait de leur forte interaction avec la matière, mais les bêtas et les gammas parurent avoir plus d’avenir en médecine et en biologie.


En octobre 1900, Giesel puis Walkoff annoncèrent que les sels de radium brûlaient la peau.Giesel plaça pendant quelques heures du radium sur son bras et nota l’évolution de la profonde brûlure que cela entraîna, observation confirmée peu après par Otto Walkoff. Elster et Geitel (inventeurs de la cellule photoélectrique) étudiaient l’ionisation de l’atmosphère et ils se rendirent compte en 1901 que l’air comme le sol étaient légèrement radioactifs. En 1901, Becquerel fut sérieusement brûlé par un échantillon de radium que lui avait confié Pierre Curie.
Celui-ci explora alors les effets biologiques du radium, d’abord sur lui-même, puis avec avec le Dr Danlos, dermatologue à l’Hôpital Saint-Louis. Il le mentionne dans son discours de réception du prix Nobel « Enfin dans les sciences biologiques les rayons du radium et son émanation produisent des effets intéressants que l’on étudie actuellement. Les rayons du radium ont été utilisés dans le traitement de certaines maladies (lupus, cancer, maladies nerveuses). Dans certains cas leur action peut devenir dangereuse. ».Thomson annonça en 1903 que l’eau, elle aussi, était radioactive (elle contient en effet du radon dissous) et cela suscita beaucoup d’intérêt pour le thermalisme dont on pensa comprendre l’origine des bienfaits.

Buvard publicitaire vantant les eaux "hyperthermales très radioactives" de Plombières (Musée Curie, Paris).
En 1903 toujours, Elster et Geitel découvrirent (en même temps que William Crookes) que le sulfure de zinc scintillait en recevant un rayon alpha. Cela permettait de compter les transmutations une par une : si leur rythme moyen était constant, leur survenue se révéla aléatoire, ce qui troubla beaucoup les physiciens.
La concurrence devenait très intense, mais les Curie gardaient une longueur d’avance. Les sources radioactives qu’ils préparaient étaient dix à vingt fois plus pures et donc plus intenses que celles de leurs rivaux, ce qui rendait beaucoup plus nets les phénomènes observés. Mais il fallait des tonnes de minerai d’uranium pour en extraire des milligrammes de radium. Ce minerai était coûteux, mais Pierre obtint à bas prix des résidus de pechblende, du minerai dont l’uranium avait déjà été extrait et qui n’avait (au début) aucune valeur marchande. Cent kilos arrivèrent à Paris début 1899, et Pierre Curie engagea André Debierne pour l’assister. Il passa également un contrat avec la Société Centrale de Produits Chimiques (société qui commercialisait déjà les instruments qu’il avait inventés). Cette société prenait en charge les premières étapes de la séparation chimique des sels radioactifs, en conservait une partie qu’elle commercialisait (les prix montaient en flèche devant une demande sans cesse accrue) et donnait le reste au laboratoire Curie qui effectuait les dernières étapes de séparation. Ce travail final demeurait cependant très lourd (Marie Curie racontera volontiers plus tard les conditions pénibles dans lesquelles elle dut travailler). Une tonne de résidus fut traitée au cours de l’été 1899, deux tonnes supplémentaires fin 1899, six en 1900, cinq en 1902.
Mais en 1903, le gouvernement autrichien décréta un embargo sur les exportations de résidus de pechblende. Les Curie furent cependant épargnés par cet embargo (à la grande fureur de leurs collègues, britanniques et allemands en particulier) et ils reçurent dix tonnes de minerai en 1904. Avec les 100 mg de chlorure de radium dont elle disposait alors, Marie Curie donna en 1902 une première estimation de la masse atomique du radium : 225±1 . La valeur actuelle est 226. Tous ces résultats lui permirent de soutenir brillamment sa thèse de doctorat en juin 1903, quelques mois avant de partager le prix Nobel de physique avec son mari, et Becquerel.

La thèse de doctorat de Marie Curie
Le prix Nobel, une nouveauté
Alfred Nobel avait créé en 1895 un prix récompensant des œuvres exceptionnelles en Physique, Chimie, Physiologie et médecine, Littérature et Paix. Les premier prix furent attribués en 1901: Röntgen reçut le prix de physique. Lorentz et Zeeman se partagèrent celui de 1902 (effets du magnétisme sur le rayonnement). Des rumeurs suggéraient que le prix de 1903 allait être partagé entre Henri Becquerel et Pierre Curie. Pierre Curie insista fortement pour que sa femme soit considérée comme son égale, et non une simple assistante → Becquerel reçut la moitié du prix et Pierre et Marie chacun un quart

Pierre Curie obtint enfin une chaire de physique à la Sorbonne et il fut admis en 1905 à l’Académie des Sciences. La chaire fut créée spécialement pour lui, axée sur la radioactivité mais lui laissant toute latitude pour aborder d'autres sujets comme les questions de symétrie ou l’ionisation des gaz car Pierre Curie songeait toujours à revenir à ses travaux de cristallographie. Il disposait enfin, rue Cuvier, d'un laboratoire correctement équipé, en instruments et il disposait surtout des sources de radioéléments particulièrement précieuses. Il put ainsi poursuivre ses recherches, en collaboration avec Marie Curie qui avait le titre de chef de travaux, et quelques élèves. Marie était depuis 1900 chargée de cours, puis professeur, à l'École Normale Supérieure de Jeunes Filles à Sèvres, où elle avait ajouté au programme de physique un enseignement de mathématiques et des travaux pratiques.
L'industrie du radium
Une partie de la fascination provoquée par le radium venait de son prix exorbitant. Dans les premiers temps, il n’était extrait que des mines de Joachimstahl en Bohême, à raison d’un gramme pour 5 à 10 tonnes de résidu de pechblende, au terme d’une longue suite d’opérations chimiques et physiques. Un industriel, Armet de Lisle, ouvrit en 1904 à Nogent-sur-Marne, avec l’aide des Curie, la première usine au monde d’extraction du radium (extrayant aussi de l’uranium, du thorium, de l’actinium, et du polonium, puisque ces éléments sont toujours présents ensemble). L’usine fonctionna jusqu’en 1928 (l’école primaire Marie Curie occupa les lieux, quelque peu contaminés, de 1968 à 1998).
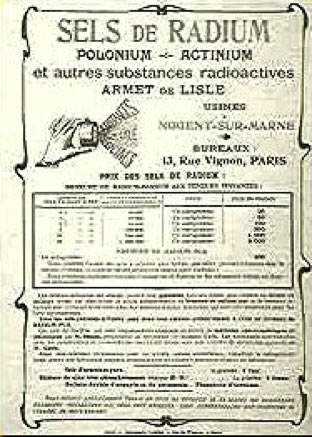
Les tarifs de l’usine d’Armet de Lisle ©ACJC
À l’échelle industrielle, Armet de Lisle installa en 1904 la première usine à Nogent/Marne. Elle effectuait les premières étapes de la séparation : une tonne de résidu de pechblende, cinq tonnes de produits chimiques cinquante tonnes d'eau de lavage → 1 à 2 mg de bromure de radium. Les produits semi-finis partaient au laboratoire Curie pour les dernières étapes. Utilisations: médicales (radium puis radon), industrielles (montres phosphorescentes…)
On estime qu’il y avait environ 4 g de radium disponibles dans le monde en 1904 (dont 1.5 en France, 1 en Allemagne, 0.5 en Grande-Bretagne et 0.5 aux États-Unis). L’embargo instauré par le gouvernement austro-hongrois déclencha la recherche d’autres gisements dans le monde. Le minerai de carnotite du Colorado permit à la Standard Chemical Co. de Pittsburgh de produire 200 g de radium en une douzaine d’années, de 1913 à 1926, la moitié à usage médical, l’autre à usage industriel (en particulier des peintures phosphorescentes pour les cadrans de montre). Le prix était alors de l’ordre de 100 000 $ (de l’époque, soit à peu près 1 M €) le gramme. C’est d’ailleurs une collecte effectuée auprès des femmes américaines qui permit d’offrir en 1921 un gramme de radium à Marie Curie.

Cristallisation fractionnée pour séparer radium et baryum à l’usine de la Standard Chemical
À la suite de la découverte en 1915 de la mine de Shinkolobwe, dans ce qui était alors le Congo Belge, l’Union Minière du Haut Katanga ouvrit en 1922 une usine près d’Anvers qui produisit de 50 à 100 g de radium par an (selon les besoins des clients), le prix diminuant de 75 000 à 25 000$ le gramme. En 1930 s’ouvrit l’Eldorado Gold Mine, à Port Hope au Canada, et les Canadiens montèrent un cartel avec les Belges (60% du marché pour les Belges, 40% pour les Canadiens). On estime qu’au total, 1 500 g de radium furent produits dans le monde jusqu’en 1940 (mais presque plus rien par la suite), dont le tiers se trouvait alors en Europe. La mine de Joachimsthal (Jachimov en tchèque) a continué à extraire du radium (à raison de 3 g par an) et surtout à livrer de l’uranium (à l’Allemagne après l’annexion des Sudètes en 1938, puis à l’URSS après 1945). C’est aujourd’hui une station thermale réputée.
Complications
Assez rapidement, les Curie se plaignirent que les mesures devenaient difficiles dans leur laboratoire car l’air y était ionisé presque en permanence. Cela faussait les délicates mesures, la radioactivité serait-elle contagieuse ? Les Curie pensèrent que des poussières riches en radium causaient ces troubles, mais cette radioactivité « induite » diminuait rapidement avec le temps, ce qui n’était pas le cas des sels de radium. Dorn découvrit que du radium émanait un gaz, que l’on baptisa faute de mieux « émanation du radium ». Il ne reçut son nom actuel de radon 222 qu’en 1923. Cette émanation laissait à son tour un dépôt radioactif sur les instruments. À Montréal, Rutherford découvrait, lui, une « émanation du thorium », appelé ensuite thoron et aujourd’hui radon 220. Cela le conduisit à découvrir la transmutation nucléaire, et à comprendre peu à peu pourquoi le radium et le polonium étaient toujours mêlés à l’uranium et au thorium, la raison de leurs proportions relatives, et de leurs différences de radioactivité.
Mais ce qui surprenait le plus les physiciens, c’était la propriété des corps radioactifs de libérer en permanence de l’énergie de façon apparemment inépuisable. Non seulement cela allait à l’encontre de la loi bien vérifiée de la conservation de l’énergie, mais il s’agissait en plus d’une énergie considérable. Dès sa note du 12 avril 1898, avait Marie Curie suggéré:

Le radium rayonne de la lumière en permanence (ou pour être exact il excite les molécules d’air qui rayonnent de la lumière) ainsi qu’une chaleur suffisante pour chauffer de l’eau : Pierre Curie et Albert Laborde mesurèrent en 1903 un dégagement constant de chaleur de l’ordre de 100 calories par gramme et par heure. Quelle pouvait être la source de cette énergie inépuisable ? En 1900, Marie Curie pensait que « le rayonnement est une émission de la matière accompagnée de la perte de poids des substances radioactives ». Prémonitoire ? Oui, mais il n’y avait pas d’indication expérimentale allant en ce sens, la perte de masse supposée n’était pas mesurable, et aucun changement de nature de l’uranium, du thorium ou du radium ne se manifestait jusque-là dans les expériences. En 1902, Pierre et Marie Curie revinrent donc à l’idée « que le radium utilise une énergie extérieure de nature inconnue », fonctionnant comme une antenne qui capterait continuellement une énergie diffuse baignant tout l’espace. Ils s’intéressaient beaucoup au spiritisme à ce moment-là, participant à des expériences avec des médiums comme Eusapia Palladino.
Rutherford penchait, lui, pour une transformation interne de l’atome, conforté en ce sens par les expériences qu’il menait alors avec Frederick Soddy et qui les conduisirent à la notion de transmutation des atomes et à l’alchimie nucléaire. En 1905, Einstein publia sa célèbre équation E = mc2, donnant une explication à l’énergie considérable libérée par les corps radioactifs au prix d’une diminution infinitésimale de leur masse. Quelle que fût l’origine de l’énergie du radium, Pierre Curie en entrevit immédiatement toutes les conséquences et il termina en 1905 sa conférence Nobel par : « On peut concevoir encore que dans des mains criminelles le radium puisse devenir très dangereux, et ici on peut se demander si l'humanité a avantage à connaître les secrets de la nature, si elle est mûre pour en profiter ou si cette connaissance ne lui sera pas nuisible. L'exemple des découvertes de Nobel est caractéristique ; les explosifs puissants ont permis aux hommes de faire des travaux admirables. Ils sont aussi un moyen terrible de destruction entre les mains des grands criminels qui entraînent les peuples vers la guerre. Je suis de ceux qui pensent avec Nobel que l'humanité tirera plus de bien que de mal des découvertes nouvelles. »
En s’inspirant du livre de vulgarisation sur la radioactivité écrit en 1909 par Frederick Soddy, le romancier Herbert-George Wells décrivit dans The World Set Free (publié début 1914 et traduit en français sous le titre La destruction libératrice) le développement de l’énergie nucléaire, et une guerre dans laquelle des bombes nucléaires seraient larguées d’avion. Il imagina au passage que la possibilité de rendre des corps artificiellement radioactifs serait mise au point en 1933 (ce n’est qu’en 1934 que les Joliot-Curie découvrirent la radioactivité artificielle !).


Le roman de H.G. Wells qui anticipe l’énergie nucléaire
La mort accidentelle de Pierre Curie en 1906 entraîna l’arrêt de nombreux travaux du laboratoire Curie consacrés à la physique de la radioactivité, et le laboratoire s’orienta plutôt vers la chimie des substances radioactives, la métrologie et les applications thérapeutiques (par un rapprochement avec l’Institut Pasteur où Jean Danysz étudiait les effets du radium sur divers organismes vivants, les bactéries en particulier).
Cela laissa le champ libre à Rutherford et ses collaborateurs pour résoudre la question de l’origine de la radioactivité, de son énergie, et de la structure de l’atome. Les « années Rutherford » changèrent directement et indirectement la face du monde, et nous y reviendrons.

Ernest Rutherford (1871-1937)
L’Institut du Radium de Paris
La mort de Pierre Curie
Le 19 avril 1906, Pierre Curie fut renversé par un camion (hippomobile) qu'il ne vit pas arriver alors qu'il traversait une rue sous la pluie, abrité par son parapluie. Il tenta de se raccrocher à l’un des percherons, mais glissa entre les sabots. La roue arrière gauche lui broya la tête, le tuant sur le coup. Le choc fut immense pour Marie qui mit plusieurs années à s'en remettre partiellement. Elle est lui succéda à sa chaire de la Sorbonne, d'abord avec le simple titre de chargée de cours (la chaire étant déclarée vacante), avant de devenir enfin professeur, deux ans plus tard . Elle fut alors la première femme professeur d'université en France. Elle obtint également la direction du laboratoire Curie, assistée d'André Debierne.

Leçon inaugurale de Marie Curie à la Sorbonne, le 5 novembre 1906.
Le premier cours de Marie Curie fut un événement mondain et le public s'y pressa en nombre. « Son cours terminé, et après avoir donné une vision de la petite lueur bleue du radium, madame Curie se retira comme elle était apparue, modeste et simple, insensible aux applaudissements et aux ovations de son auditoire » rapporta L’Illustration tandis que Le Journal y vit une grande victoire du féminisme : « Le temps est proche où les femmes deviendront des êtres humains. » D'autres virent cependant un objet de scandale dans cette place faite à une femme, d'origine étrangère qui plus est.
L'Institut du Radium

Émile Roux, directeur de l’Institut Pasteur, proposa en 1909 à Marie Curie la création conjointe avec l’université d’un institut destiné à l’étude du radium. Grâce à un legs de D. Osiris, l’Institut du Radium fut inauguré en 1914. Il était formé de deux pavillons: le pavillon Curie où devaient être étudiées les propriétés physiques de la radioactivité, et le pavillon Pasteur consacré aux applications médicales sous la direction de Claudius Regaud (1870-1940), pionnier de la radiothérapie.

Le Pavillon Pasteur avec les bustes de Marie et Pierre Curie
Un dispensaire fut ajouté en 1923, puis un hôpital en 1936. L’Institut du Radium est devenu Institut Curie en 1970.
Turbulences et honneurs
Affaire Langevin
Premier Congrès Solvay (1911)

Marie Curie dans son laboratoire

Prix Nobel de chimie 1911
Le curie, unité de radioactivité = nombre de désintégrations par seconde dans un gramme de radium [en principe en l’honneur de Pierre]: 1 curie (Ci) = 107 becquerels (Bq)

Les « petites Curie »: unités mobiles de radioscopie pendant le 1° guerre mondiale.
Irène Curie

Irène et Marie Curie en 1921 à l’Institut du Radium
« Le gramme de radium », une belle opération de relations publiques

Marie Curie et le président des États-Unis Warren Harding en 1921
Dernières années

Marie Curie en 1921
Devenue une légende
« J'ai retiré ce radium de la pechblende Et j'ai brûlé mes doigts à ce feu défendu » Aragon (Les yeux d’Elsa 1942)


Hommage à Marie Curie par Google
Quelques une des nombreuses biographies consacrées à Marie Curie (et occasionnellement à Pierre Curie):
 |
 |
 |
 |
 |
 |
 |
|---|---|---|---|---|---|---|
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
 |
Radiofolies
Les premières applications de la radioactivité furent médicales. Et ludiques ! Les rayons X avaient provoqué un immense engouement et un émerveillement populaire. La radioactivité possédait la même aura mystérieuse, et le radium la symbolisait plus que tout. Il fut l’objet d’un véritable emballement qui persista pendant des décennies. La « Petite boutique du radium » expose au musée Curie, à Paris, tout un éventail d’applications des plus farfelues aux plus sérieuses, des plus inoffensives aux plus dangereuses.

La Petite boutique du radium au musée Curie à Paris
Ce radium qui brillait dans l’obscurité était d’ailleurs si impressionnant que la célèbre photographie qui le montrait servit au timbre émis en 1967 pour le centenaire de la naissance de Marie Curie.

Photo prise à la seule lueur du radium. La lumière ne vient pas directement du radium mais des molécules d’air excitées par son rayonnement. ©ACJC

Timbre en l’honneur de Marie Curie émis en 1967 pour le centenaire de sa naissance
En dehors des Curie, personne ne disposait alors d’assez de radium pour admirer ce spectacle, mais un jouet scientifique fit fureur à la Belle Époque, le spinthariscope de Crookes. Ayant découvert que le sulfure de zinc scintillait sous le choc des rayons alpha, il eut l’idée de mettre une très petite quantité de radium à proximité d’un écran de sulfure de zinc, à l’intérieur d’un tube fermé par une lentille grossissante permettant d’observer les scintillations.

Spinthariscope de 1910 (modèle de Crookes) au radium

Spinthariscope moderne à l’uranium © Th.W. Gray
Ce n’était pas seulement un jouet : un écran de sulfure de zinc soumis à un rayonnement intense paraît uniformément éclairé, mais quand l’intensité diminue, il se met à ressembler à une « mer lumineuse turbulente », puis à une intensité encore plus faible, l’écran scintille sans cesse en allumant des éclairs de façon apparemment aléatoire. Chacun de ces minuscules éclairs correspond à la transmutation d’un seul atome de radium : on voit donc littéralement et le caractère atomique de la matière et le caractère aléatoire du monde quantique ! Cela dit, c’était aussi un jouet :



Spinthariscope jouet de 1947, et sa publicité
Poésie, théâtre et littérature s’emparèrent également du sujet. Si H.G. Wells annonça l’énergie nucléaire en 1914 dans The world set free, dès 1908 Anatole France évoqua dans L’île des pingouins une bombe à base de radium (ou plutôt de radon). En 1936, Céline imagina dans Mort à crédit un héros passionné par l'agriculture "radiotellurique". Paul d’Ivoi, grand auteur de romans populaires, écrivit La course au radium et Le roi du radium (réédité sous le titre Le radium qui tue) qui évoque le laboratoire des Curie et les expériences de Crookes sur le spiritisme.


Les romans d’aventures de Paul d’Ivoi ont toujours des lecteurs
Et le radium est bien sûr demeuré présent dans les bandes dessinées, jusqu’à nos jours :

On ne cherchera pas ici d’exactitude scientifique, le radium n’émettant pas de rayons X, et les rayons X n’étant pas visibles à l’œil nu.
Les sources thermales vantèrent dès le début du XX° siècle la radioactivité naturelle de leurs eaux : à Vichy, Plombières et dans bien d’autres stations, l’eau jaillit légèrement radioactive, et comme la radioactivité apparaissait alors comme une source de vie, elles axèrent leur « réclame » sur cette particularité. Et comme l’effet bénéfique semblait diminuer avec le transport (ce qui était attribué à la courte période de 92 h du radon), on vendit aussi de nombreuses « fontaines au radium » pour irradier chez soi l’eau des boissons, ou même des bains.


Deux modèles de fontaine au radium, pour irradier l’eau de boisson (Musée Curie, Paris)
Comme il n’est pas exclu qu’une (faible !) dose de radioactivité puisse être bénéfique pour l’organisme (théorie de l’hormesis), Jáchymov (ancienne Joachimsthal) prise toujours très haut son radon:


Dépliant publicitaire contemporain vantant le radon des eaux de Jachymov
Les bienfaits supposés du radium, et plus généralement de la radioactivité, ne pouvaient pas échapper à l’industrie pharmaceutique, et l’on vit apparaître quantité de produits « à base de radium », pour soigner aussi bien la bronchite voire la tuberculose (Tubéradine), que les troubles digestifs (Digéraline), l’anémie ou la fatigue (Vigoradine, Radiovie). On en fit des poudres et des crèmes de beauté, des savons, dentifrices, shampooings, des boissons tonifiantes et rajeunissantes. On fabriqua des compresses Radiumcure, une laine Oradium pour la layette des bébés (en raison de ses « extraordinaires effets de stimulation organique d'excitation cellulaire transmis par le radium »), des oreillers pour un sommeil réparateur. Les animaux n’étaient pas oubliés : le Provaradior était un aliment pour bétail, « Le Radia, appât radioactif, attire les poissons et écrevisses comme l'aimant attire le fer. » Les plantes n’étaient pas négligées non plus, et l’on vendait des engrais radioactifs pour stimuler leur croissance.


Le radium était si merveilleux qu’il pouvait à la fois faire repousser les cheveux (avec la lotion capillaire au radium du Dr. Rezall) et débarrasser des poils superflus et des maladies cutanées. À vrai dire, il était nettement plus efficace dans ce second rôle, mais non sans danger. En 1932, un certain docteur Alfred Curie déposa à Paris la marque Tho-Radia (thorium-radium) et commercialisa toute une gamme de produits de beauté, préparés par le pharmacien Alexis Moussali (qui avait auparavant commercialisé les Laboradium, Microradium, Radiobust, Radiofluide, Radioskin, RadiumCure, et Radiviril). Le Dr Alfred Curie n’avait aucun lien de parenté avec Pierre Curie, mais les produits auxquels il prêtait son nom eurent un certain succès. La radioactivité des 0.25 microgrammes de bromure de radium que contenait la crème (pour 100g d’excipient) n’était pas très dangereuse : le prix colossal du radium protégeait les acheteuses !



La société Tho-Radia avait une gamme complète de produits de beauté (Musée Curie, Paris)
Mais ce ne fut pas toujours le cas. Un milliardaire américain, Eben Byers, mourut en 1932 empoisonné au radium après avoir consommé en quatre ans des milliers de flacons de Radithor, contenant chacun une microcurie de radium 226 et une de radium 228 (alors appelé mésothorium) dans de l’eau distillée. Le Radithor était censé soigner tout un éventail de troubles variés, dont la fatigue et l’impuissance, mais chaque petit flacon avait une activité de 74 kBq, et en en consommant plusieurs par jour, Eben Byers finit par accumuler près de 350 sieverts (le radium se fixe dans les os).

Le Radithor (© Th. Gray)
À la même époque, une autre affaire tragique, celle des « Radium girls », attira aussi l’attention du public sur les dangers de la radioactivité. L’idée vint dès 1902 de fabriquer une peinture « phosphorescente » en mélangeant un peu de radium à du sulfate de zinc et de l’huile de lin. L’industrie horlogère se mit à sortir en série des montres dont les aiguilles et le cadran étaient lisibles de nuit. L’armée était particulièrement intéressée, et marché explosa avec la Première Guerre Mondiale.

Une montre à chiffres et aiguilles lumineux
Aux États-Unis, l’U.S. Radium Corporation agrandit son usine et s’installa en 1921 à Orange, dans l’Illinois, utilisant plusieurs dizaines de jeunes femmes à peindre les chiffres et les aiguilles. Pour plus de précision, elles affinaient sans hésiter leur pinceau du bout de la langue. Beaucoup d’entre elles développèrent des cancers de la bouche et de la gorge et des nécroses de la mâchoire, et plusieurs en moururent.

Ouvrières de l’usine d’Orange (Illinois) vers 1920 © Argonne National Laboratory
Le radium était clairement la cause de ces cancers mais, pour que leurs droits soient reconnus, il fallut que cinq des victimes, les Radium girls, recourent à un procès difficile auquel elles survécurent peu de temps. Ce procès marqua d’ailleurs un grand pas en avant dans la reconnaissance des risques professionnels aux USA. Il aida également à fixer en 1941 pour le radium une première norme de sécurité avec une dose maximale annuelle de 0.1 µCi (3.7 kBq), alors que les ouvrières avaient absorbé des milliers voire des dizaines de milliers de fois cette dose.

Dessin paru le 28 février 1926 dans le supplément dominical de l’American Weekly
Les peintures au radium ont disparu, le radium étant désormais remplacé par du tritium ou de l’américium beaucoup moins nocifs. Mais la culture populaire se souvient de ces montres :

Radiothérapie
Les rayonnements blessent, ils guérissent aussi. Les effets biologiques nocifs du radium sur la peau ayant été très vite découverts, à la suite des expériences douloureuses de Giesel, Walkoff, Becquerel, Curie, l’idée vint immédiatement d’en rechercher des effets bénéfiques. Pierre Curie prit contact avec le Dr Henri Danlos, dermatologue à l’Hôpital Saint-Louis à Paris, qui fit des tentatives de traitement du lupus par le radium (on avait déjà employé les rayons X à cet effet). Dans de nombreux pays, les médecins multiplièrent les essais sur d’autres pathologies, avec des succès mitigés. Le radium se révéla inefficace contre la tuberculose, très répandue alors, mais il conduisit à des résultats encourageants sur les tumeurs cutanées. Le traité de radiothérapie de Joseph Belot, apparu en 1905, couvrait les applications des rayons X et du radium. Bergognié et Tribondeau montrèrent en 1906 que les cellules à multiplication rapide étaient plus sensibles que les autres aux rayonnements ionisants, expliquant l’efficacité des rayons X et gamma pour traiter les cancers. Pendant un demi-siècle, le traitement de certains cancers fut donc la principale application médicale de la radioactivité.
Premiers efforts
L’idée a toujours été de déposer la dose maximale de rayonnements pour « tuer » les cellules cancéreuses en épargnant autant que possible les cellules saines environnantes. Les rayonnements pénètrent d’autant plus profondément qu’ils ont une grande énergie, d’où une augmentation régulière de la puissance des tubes à rayons X (tubes de 50 kV, 100 kV, 300 kV) mais la technique avait ses limitations et on n’utilisa les rayons X (röntgenthérapie) que pour les tumeurs superficielles. Les rayons gamma du radium (ou du radon) avaient plus d’énergie et ils servirent pour les tumeurs un peu plus profondes (curiethérapie ou brachythérapie). Leur énergie n’était cependant ni modulable ni très élevée, d’où le remplacement du radium après 1950 par d’autres sources radioactives comme le cobalt ou l’iridium. De plus, les rayonnements déposent leur énergie dès leur entrée dans les tissus : ils permettent donc de traiter des tumeurs superficielles en plaçant la source radioactive à proximité immédiate.

Une tumeur superficielle localisée (en rouge) peut être traitée en plaçant à son contact immédiat une source radioactive (en jaune). Une tumeur interne peut être traitée de la même façon si une cavité naturelle se trouve à proximité (cancer du col de l’utérus par exemple), ou si la source radioactive peut être insérée dans la tumeur (cancer de la prostate).
Pour traiter des tumeurs profondes, il fallait augmenter l’intensité du rayonnement (donc la quantité de matière radioactive) pour qu’une dose suffisante pénètre jusqu’à la tumeur, mais les tissus placés sur le chemin risquaient d’être complètement brûlés. La solution fut la « bombe » au radium, dans laquelle une forte quantité de radium (jusqu’à plusieurs grammes) était placée au cœur d’un blindage ne laissant s’échapper qu’un mince faisceau. La « bombe » pivotait tout autour du patient en gardant le faisceau braqué vers la tumeur : celle-ci était ainsi continuellement bombardée tandis que les tissus intermédiaires ne recevaient qu’une fraction de la dose totale. Ce principe est toujours utilisé dans les « bombes au cobalt » et les accélérateurs de particules qui ont remplacé les bombes au radium à partir des années 50.

Bombe au radium de l’Institut du radium en 1934 ©ACJC

Principe d’une « bombe » au radium : la source (en jaune) est entourée d’un blindage qui ne laisse passer qu’un faisceau (en bleu) pointé sur la tumeur (en rouge). La source pivote autour du patient pour minimiser l’irradiation des tissus sains.
Les idées sur le cancer avaient très vite évolué à la fin du XIX° siècle. Considéré depuis Galien comme une maladie « constitutionnelle » de l’ensemble de l’organisme avec des manifestations locales, le cancer était désormais considéré comme une maladie locale touchant les cellules de certains tissus, et son traitement passa des mains des médecins à celles des chirurgiens. L’évolution de la société (occidentale) faisait par ailleurs du cancer un problème grandissant de santé publique. La question s’est très vite posée de savoir si la radiothérapie devait être un outil à la disposition des chirurgiens qui traitaient une tumeur comme une maladie particulière d’un organe (gynécologues pour les cancers de l’utérus, dermatologues pour ceux de la peau) ou si elle devait être une spécialité à part entière, les radiothérapeutes soignant tous les cancers quelle que soit leur localisation. Une seconde controverse se greffa sur celle-ci : le seul traitement des cancers était alors la chirurgie, mais beaucoup de tumeurs n’étaient pas opérables, et les chirurgiens voyaient dans la radiothérapie au mieux un traitement palliatif pour les cas désespérés. Ces questions de pouvoir divisèrent longtemps le monde médical et se résolurent différemment d’un pays à l’autre.

Une affiche britannique de lutte contre le cancer © Games
De grands centres de recherche anticancéreuse intégrant des services de soins par radiothérapie furent créés, le plus souvent avec un très fort soutien de philanthropes. À Londres, le Marsden Hospital, créé dès 1851 pour soigner le cancer, devint Royal Marsden Hospital en 1910 et intégra la radiothérapie. À New York toujours, le Cancer Hospital (devenu en 1948 le Sloan-Kettering Memorial Hospital) devint le plus grand centre anticancéreux privé au monde. En Allemagne, malgré la création précoce de l’Institut de recherche sur le cancer (Institut für Krebsforschung), la radiothérapie demeura du ressort des chirurgiens. La création de grands centres était justifiée par le coût exorbitant du radium, car il semblait peu judicieux de disperser les maigres quantités disponibles, et par les dangers liés à sa manipulation, que l’on ne pouvait donc confier qu’à des personnels spécialisés ayant reçu une formation adaptée. Le premier Institut du Radium, l’Institut für Radiumforschung de Stefan Meyer à Vienne, construit entre 1908 et 1910, se consacra essentiellement à la physique et à la chimie de la radioactivité, tout comme celui de l’Académie des Sciences de Russie à Saint-Pétersbourg (devenu Institut Khlopin du Radium, Радиевый институт им. В.Г. Хлопина, en 1922 en intégrant plusieurs autres centres de recherches sur la radioactivité) où travaillèrent de grands noms de la physique nucléaire russe comme Gamow, Kapitsa ou Kourtchatov. Par contre, la Grande-Bretagne, les États-Unis et le Canada fondèrent des Instituts du Radium à vocation médicale : le Radium Institute de Londres ouvrit en 1911, avec comme objectif premier les maladies de la peau, celui de New York en 1914, celui de Montréal en 1923. À Stockholm, le Radiumhemmet, créé en 1910, fut étroitement associé à la clinique chirurgicale de l’Université Karolinska.

Le pavillon Curie de l’Institut du Radium de Paris
La France fit les deux : l’Institut du Radium de Paris, aujourd’hui Institut Curie, associa dès sa conception recherches en physique, chimie, biologie et médecine. Marie Curie avait succédé en 1906 à Pierre Curie comme professeur à la Sorbonne, et elle reprit aussi son intérêt pour les applications médicales de la radioactivité. Après de difficiles tractations, et grâce à un donateur généreux et au soutien de l’Institut Pasteur et de l’Université de Paris, l’Institut du Radium fut créé en 1909. Deux pavillons furent construits : le pavillon Curie était destiné à la recherche sur la physique et la chimie de la radioactivité, sous la direction de Madame Curie, le pavillon Pasteur était destiné aux recherches sur les applications biologiques de la radioactivité, sous la direction de Claudius Regaud. L’Institut du Radium commença à fonctionner après la première guerre mondiale, et les progrès de la recherche biomédicale conduisirent ses dirigeants à créer en 1920 la Fondation Curie pour financer et gérer un dispensaire de soins pour les malades. Ouvert en 1922 à côté de l’Institut du Radium, ce dispensaire fut remplacé dès 1936 par un hôpital en raison des besoins grandissants.

Le dispensaire de la Fondation Curie, à Paris

L’hôpital qui le remplaça. ©Institut Curie
Le deuxième centre de radiothérapie anticancéreuse fut ouvert par Victor Bérard à l’Hôtel-Dieu de Lyon, en 1923. Parallèlement, Gustave Roussy, un des promoteurs de la cancérologie en France ouvrit en 1919 à l’Hôpital de l’Institut Pasteur une consultation pour malades cancéreux et un service de radiothérapie, avant de fonder l’Institut du Cancer en 1925 à l’hôpital Paul Brousse de Villejuif, réunissant des laboratoires de recherche et un hôpital. L’Institut du Cancer de Villejuif prit le nom d’Institut Gustave Roussy à la mort de son fondateur.

L’Institut du Cancer de Villejuif en 1926 © IGR
La lutte contre le cancer remplaça peu à peu la lutte contre la tuberculose comme objectif de santé publique principal, et la radiothérapie devint, à côté de la chirurgie, un moyen essentiel dans ce combat : les deux tiers des cancers sont aujourd’hui traités (au moins en partie) par radiothérapie La Ligue contre le Cancer fut fondée en avril 1918. Sur la proposition de Claudius Regaud et Jean Bergonié, le ministère de la santé organisa en novembre 1928 un réseau national de Centres anticancéreux associant recherche et soins. Une ordonnance du Général De Gaulle les réorganisa en 1945 sous la forme de 18 centres régionaux et de deux centres nationaux (qui portent aujourd’hui les noms d’Institut Curie et d’Institut Gustave Roussy). Parallèlement de très nombreux hôpitaux et cliniques ouvrirent des services de radiologie et de radiothérapie au fur et à mesure que les techniques devenaient moins coûteuses et plus maîtrisées (bien que des incidents, voire des accidents graves, arrivent encore).
Röntgenthérapie, Curiethérapie et les autres
Les médecins avaient très vite compris que les rayonnements ionisants tuaient plus facilement les cellules cancéreuses que les cellules saines, bien qu’ils n’aient pas su pourquoi. Mais il y eut un long chemin à parcourir avant qu’ils ne parviennent à optimiser les doses de ces rayonnements tout en minimisant les risques pour les patients (et les opérateurs !). À l’âge héroïque, il n’était pas possible de calculer la dose de rayonnement émise (et encore moins la dose reçue), et les médecins recouraient le plus souvent à une irradiation massive aux rayons X d’une grande partie du corps pour détruire la tumeur d’un seul coup. Cela entraînait fréquemment la nécrose des tissus sains environnants sans garantir l’absence de récidive de la tumeur. Pour les tumeurs traitées par radioactivité, on employait des sels de radium, d’abord contenus dans des tubes en verre puis dans des aiguilles en platine, placés contre les tumeurs (ou à l’intérieur) ce qui limitait leur usage aux cancers accessibles de l’extérieur et de petite taille (cancers du sein, de la peau, du col de l’utérus). Le radium coûtant très cher, on a utilisait plutôt son descendant, le radon 222. Celui-ci est produit en continu par le radium, il se désintègre en quelques jours et des gammas apparaissent dans la transmutation bêta de son descendant le plomb 214. On recueillait le radon dans des tubes moins risqués à transporter que la source de radium.

Source de radium à l’extrémité à l’extrémité d’une aiguille de platine (qui absorbe les bêtas et les gammas mous) © IAEA

Une boîte d’aiguilles au radium © ANDRA

Container en plomb pour le transport d’aiguilles de radium © Oak Ridge National Laboratory
En France, les pionniers de la radiothérapie furent Claudius Regaud et Gustave Roussy. Regaud avait découvert la sensibilité particulière de certains organes aux rayonnements ionisants et avait appliqué ces observations au traitement du cancer. Avec ses collaborateurs, comme Antoine Lacassagne et Henri Coutard, il mit au point à l’Institut du Radium de Paris des matériels nouveaux et élabora des protocoles de traitement pour choisir au mieux l’intensité, la durée et la fréquence des irradiations. François Baclesse jeta en 1936 les bases du traitement conservateur du cancer du sein (une radiothérapie avant la chirurgie permettait d’éviter l’ablation totale du sein). Jean Pierquin mit au point les aiguilles au radium, Lucien Mallez et Robert Collez les premières mesures dosimétriques. Les calculs de dose demeuraient empiriques, et utilisaient comme unité le milligramme de radium par heure, ce qui mesure l’activité de la source mais non la dose absorbée par les tissus (c’est toute la différence entre becquerels et grays). Avec Simone Laborde, Gustave Roussy fut également un des pionniers de l’utilisation du radium en cancérologie, d’abord en traitement de contact (curiethérapie, radiothérapie de contact, radiothérapie interne ou brachythérapie) puis en traitement à distance (radiothérapie externe ou téléradiothérapie) en mettant en place des « bombes » au radium. Les premières furent mises en service en 1929 malgré leur coût exorbitant (l’équivalent de plusieurs millions d’euros).

Claudius Regaud (1870-1940) ©ACJC

Gustave Roussy (1874-1948) © IGR
Leurs travaux conduisirent à fractionner les doses et à mettre au point des procédures standardisées pour permettre une étude fiable des relations entre doses reçues et effets biologiques. La meilleure dose pour traiter un cancer et la meilleure manière de délivrer cette dose faisait en effet l’objet de nombreuses études semi-empiriques. Hermann Wintz (1887-1947) et Guido Holzknecht (1872-1931) préconisaient par exemple de délivrer une dose aussi intense que possible dans le délai le plus court possible, tandis que Leopold Freund (1868-1943) et Claudius Regaud favorisaient le fractionnement des doses. Robert Kienböck (1871-1953) insista sur la nécessité de mesurer les doses délivrées. Les Suédois mirent au point le « système de Stockholm » dans lequel des doses de 30 à 90 mg de radium étaient appliquées pendant 24 h à 2 ou 3 reprises, espacées d’une semaine. Le « système de Paris » (premier du nom) employait initialement une seule application de 60 mg de radium laissés 5 jours en place. À New York, Edith Quinby (1891-1982) fut l’une des premières à déterminer la distribution du rayonnement produit par les aiguilles de radium selon leur disposition, permettant de rechercher la disposition la plus efficace selon la tumeur à traiter. Elle compara aussi les effets des rayonnements bêta et gamma, et elle élabora en 1941 la première table de traitement reliant dose émise et dose reçue. Ses travaux conduisirent James Ralston Paterson (1897-1981) et Herbert Parker (1910-1984) à mettre au point à partir de 1934 le « système de Manchester » dans lequel la position des tubes de radon ou des aiguilles de radium était très précisément définie pour maximiser la dose reçue par la tumeur (en particulier celle du col de l’utérus) tout en minimisant la dose reçue par les cellules saines autour. Parker rejoignit ensuite les Etats-Unis où il dirigea la section médicale des laboratoires nucléaires d’Oak Ridge puis de Hanford, y mettant au point les doses admissibles de radioactivité et y définissant le rem (Röntgen equivalent man, ancêtre du sievert) à partir de la dose reçue (en rad, ancêtre du gray).

Edith Quinby (1891-1982)
La radiothérapie devint une technique reconnue près le rapport de Henri Coutard (1876-1950) répertoriant les résultats positifs. La technique progressait également, les tubes à rayons X montant désormais à 200 kV permirent de traiter efficacement des cancers superficiels (le faisceau pénétrant jusqu’à quelques centimètres de profondeur). Les séances de radiothérapie demeuraient extrêmement longues et pénibles. Une solution fut d’augmenter la charge de radium des bombes (on atteignit 15 puis 50 grammes), ce que la baisse (modérée) du prix du radium rendit plus facile. La découverte de la radioactivité artificielle par Irène et Frédéric Joliot-Curie en 1934 ouvrit de nouveaux horizons. Il devenait possible de fabriquer quasiment à la demande la source radioactive ayant l’intensité et l’énergie voulue pour telle ou telle application. On put également choisir des éléments à courte durée de vie, disparaissant donc rapidement, ou des éléments ayant les propriétés biochimiques voulues pour s’installer d’eux-mêmes précisément à l’endroit voulu pour le traitement (radiothérapie métabolique). L’iridium 192 (bien plus facile à modeler en fils prenant la forme voulue) et le césium 137 remplacèrent le radium en radiothérapie de contact, et le cobalt 60 le remplaça dans les bombes à partir de 1951 (en France, la première fut installée en 1955 à l’Institut Gustave Roussy).

Bombe au cobalt dans les années 1960 au Centre François Baclesse de Caen ©CFB

Source de 1000 curies de cobalt 60 (dans la capsule d’inox, et son blindage ouvert) © Oak Ridge National Laboratory
Une grande partie de ces développements se déroula d’ailleurs en France, en particulier à l’Institut Gustave-Roussy de Villejuif, sous l’impulsion de Maurice Tubiana et de Jean Dutreix pour la radiothérapie externe, d’Andrée Dutreix pour la dosimétrie, et de Bernard Pierquin pour la curiethérapie. Maurice Tubiana y développa en particulier l’utilisation des isotopes radioactifs, comme l’injection d’iode 131 pour le traitement du cancer de la thyroïde. Dans les années 1960, Bernard Pierquin et Andrée Dutreix développèrent le « système de Paris » (deuxième du nom) en fournissant des règles d’implantation rigoureuses de l’iridium 192 et une dosimétrie prévisionnelle permettant de déposer 60 grays dans le volume de la tumeur en 3 à 10 jours d’irradiation continue (ou en deux ou trois fractions).

« Grains » d’iridium 192 utilisés en curiethérapie ©NIH
Les sources radioactives émettrices de rayons bêta se virent aussi remplacés à partir de 1952 par des accélérateurs d’électrons (les bêtatrons) permettant de régler avec précision le flux et l’énergie des rayons. Toutes ces sources plus intenses permirent de diminuer les durées de traitement et d’améliorer grandement les pronostics.

Les trois méthodes d’utilisation de radioéléments pour soigner les cances : radiothérapie externe (rayons X puis « bombes » et accélérateurs), radiothérapie interne ou curiethérapie (aiguilles de radium puis fils ou grains d’iridium) et radiothérapie métabolique (comme l’injection d’iode).
D’immenses progrès ont eu lieu au cours des dernières décennies grâce d’une part à une bien meilleure connaissance des effets biologiques des rayonnements et d’autre part grâce aux progrès techniques qu’ont représenté l’association de sources intenses, de l’imagerie en temps réelle (scanners, TEP) et de l’utilisation d’ordinateurs tant pour effectuer les calculs de dosimétrie que pour piloter les sources. Mais ceci est une autre histoire…
N’oublions pas également le développement remarquable de l’utilisation de sources radioactives non pour traiter mais comme traceurs biologiques. L’ironie veut que le point de départ ait été l’incapacité l’incapacité de George de Hevesy (1885-1966) à séparer chimiquement en 1911 le « radium-D » du plomb. À cette époque le réseau des chaînes de désintégration était très mal connu, et les produits de désintégration successifs du radium s’appelaient tout bêtement radium-A, radium-B, etc. Le radium-D est en fait du plomb, mais c’est l’isotope radioactif plomb 210 du plomb ordinaire (plomb 206 ou radium-G). Hevesy pensa alors que si le radium-D avait le même comportement chimique que le plomb, il aurait le même comportement biologique, et qu’il pourrait alors suivre le métabolisme du plomb dans un organisme vivant en suivant le cheminement de la radioactivité. C’était l’idée même des traceurs radioactifs. On dit qu’il l’utilisa en particulier pour suivre au fil des jours, dans la pension de famille où il résidait, la transformation du rôti en ragoût puis en hachis puis en soupe. La découverte de la radioactivité articifielle permit d’élargir considérablement la gamme des isotopes radioactifs utilisables, et leur utilisation va aujourd’hui de la médecine (diagnostics et imagerie médicale) à la biologie, l’industrie et l’écologie.

Explorations fonctionnelles des principaux organes à l’aide de quelques radiotraceurs © Philippe Bruyant, Université Lyon I
Radioprotection
Les effets biologiques des rayonnements ionisants
Les effets biologiques de la radioactivité, et plus généralement des rayonnements ionisants, ont attiré l’attention dès leur découverte. Les brûlures de la peau dues aux rayons X furent très vite remarquées, les cancers un peu plus tard en raison de leur période de latence. Les rayonnements ionisants (rayons alpha, bêta et gamma, et rayons X) arrachent des électrons aux atomes (ils les ionisent). Dans une cellule vivante, ils peuvent rompre des molécules comme l’ADN, directement ou par l’intermédiaire des radicaux libres qu’ils contribuent à former. Les dégâts provoqués dépendent de l’énergie du rayonnement, de sa nature (les alphas interagissent fortement, donc sur une courte distance, bêtas et gammas moins, mais sur une profondeur plus grande), de la cellule touchée (les cellules en phase de multiplication sont plus vulnérables car l’ADN est moins protégé), et, bien entendu, de l’intensité de la dose reçue et de son débit. À forte dose et fort débit, les mécanismes normaux de réparation cellulaire sont saturés et la cellule meurt. À faible dose et faible débit, ces mécanismes parviennent à réparer les dégâts. La réparation est parfois incomplète et le fonctionnement de la cellule peut en être altéré. Les effets biologiques sont donc inévitables à forte dose (« déterministes ») et aléatoires à plus faible dose (« stochastiques »).
Les effets des rayonnements ionisants sur le vivant ont été très vite connus : les rayons X endommageaient la peau des premiers radiologues, et le radium a été très vite utilisé pour soigner des cancers. Les effets se révèlent très variables selon le type de rayonnement, selon les cellules touchées, selon la dose reçue et selon la durée pendant laquelle a été reçue cette dose. Ce n’est pas très surprenant puisque la même énergie est répartie sur quelques cellules pour les alphas, quelques milliers de cellules pour les bêtas et plus encore pour les gammas.
 Les rayonnements ionisants modifient les molécules
essentielles au fonctionnement cellulaire en brisant des liaisons chimiques.
Ils peuvent créer des radicaux libres, dont la réactivité chimique est très
forte et qui sont capables d’oxyder des protéines, ou les lipides des membranes
cellulaires. Ils peuvent aussi briser l’un des brins de la double hélice de
l’ADN, voire les deux, ou les liaisons entre les deux brins. Tous ces effets
sont semblables à ceux d’autres « agressions » des cellules comme une
élévation de température, une déshydratation, la présence de substances
toxiques, ou l’activité des radicaux libres dus à la respiration cellulaire.
Ces agressions sont très fréquentes (on estime que l’ADN subit constamment un
millier de lésions par heure et par cellule) et elles sont sans doute à
l’origine du vieillissement cellulaire. Les cellules disposent fort
heureusement de mécanismes de réparation très efficaces. Ainsi, lorsqu’un seul
brin de l’ADN est brisé, la réparation prend le brin intact comme modèle.
Lorsque les deux brins sont brisés, la recopie n’est plus possible, et la
cellule déclenche une sorte de « suicide cellulaire » appelé
apoptose.
Les rayonnements ionisants modifient les molécules
essentielles au fonctionnement cellulaire en brisant des liaisons chimiques.
Ils peuvent créer des radicaux libres, dont la réactivité chimique est très
forte et qui sont capables d’oxyder des protéines, ou les lipides des membranes
cellulaires. Ils peuvent aussi briser l’un des brins de la double hélice de
l’ADN, voire les deux, ou les liaisons entre les deux brins. Tous ces effets
sont semblables à ceux d’autres « agressions » des cellules comme une
élévation de température, une déshydratation, la présence de substances
toxiques, ou l’activité des radicaux libres dus à la respiration cellulaire.
Ces agressions sont très fréquentes (on estime que l’ADN subit constamment un
millier de lésions par heure et par cellule) et elles sont sans doute à
l’origine du vieillissement cellulaire. Les cellules disposent fort
heureusement de mécanismes de réparation très efficaces. Ainsi, lorsqu’un seul
brin de l’ADN est brisé, la réparation prend le brin intact comme modèle.
Lorsque les deux brins sont brisés, la recopie n’est plus possible, et la
cellule déclenche une sorte de « suicide cellulaire » appelé
apoptose.
Dommages infligés à l’ADN par des rayonnements UCAR University of Michigan
La réparation cellulaire parvient à compenser les effets d’une faible dose de radiation, surtout si elle est étalée dans le temps, mais elle est saturée en cas de dose importante délivrée pendant un court laps de temps. Les cellules qui ne parviennent pas à être réparées meurent et les tissus se nécrosent. Si la nécrose n’est pas trop étendue, l’organisme parvient à l’éliminer, et à remplacer les cellules mortes, sinon une lésion inflammatoire apparaît, comme lors d’une brûlure, et des pathologies apparaissent.
Parfois la réparation est incomplète mais la cellule survit quand même, avec des modifications. Quand ces modifications touchent l’ADN, elles se transmettent lors de la division cellulaire. Il y a eu une mutation. Cela survient lors d’une irradiation intense : le système de réparation est saturé mais il ne peut pas « tuer » trop de cellules au risque de mettre en danger la survie de l’organisme. Il laisse alors survivre des cellules mutées qui peuvent conduire à un cancer quand le contrôle de leur division est altéré. C’est l’origine des cancers radio-induits. En fait, les cellules interagissent de façon très complexes les unes avec les autres. Dans certains cas, les cellules saines peuvent bloquer le développement des cellules cancéreuses, mais l’inverse est également possible. L’effet des rayonnements est donc beaucoup plus complexe qu’un simple effet balistique de brisure d’un brin d’ADN par un rayon alpha ou bêta, puisqu’il met aussi en jeu tout un réseau d’interactions subtiles avec le reste de la cellule et avec les cellules voisines.

Cassures double brin (en orange) par irradiation alpha de l’ADN (en vert) de kératinocytes CNRS-CENBG
Les mécanismes provoquant les cancers à la suite d’une irradiation étant identiques à ceux qui provoquent des cancers à la suite d’agressions chimiques ou traumatiques, ce n’est qu’au terme d’études statistiques que l’on peut déceler l’influence d’irradiations, en détectant un excès de cancers d’un type donné pour certaines populations. Mais il est impossible de déterminer l’origine d’un cancer donné. La complexité de l’enchaînement des mécanismes qui relie l’irradiation au cancer fait que l’étude de l’impact des rayonnements sur tel ou tel organe a surtout été menée au travers de ces études statistiques, en particulier auprès des radiologues du début du XXe siècle, des travailleurs du nucléaire et surtout des survivants d’Hiroshima et Nagasaki.
Les tissus les plus sensibles aux rayonnements sont les tissus où le renouvellement cellulaire est rapide : c’est le cas des embryons, des cellules génitrices, ou de celles de la moelle osseuse. Les enfants présentent aussi une sensibilité plus grande à l’irradiation. Inversement, les cellules qui ne se divisent peu et lentement ont une plus grande résistance à l’irradiation. Mais l’accumulation de doses relativement faibles sur une longue durée peut avoir des effets tardifs sur ces tissus, comme les fibroses de la peau des radiologues ou l’opacification du cristallin dont souffrit Marie Curie. Inversement, c’est parce que les cellules cancéreuses se multiplient rapidement qu’elles sont particulièrement sensibles aux rayonnements (bêta et gamma surtout), ce qui est à la base de la radiothérapie.
L’existence de pathologies non cancéreuses induites par les rayonnements a aussi été repérée au travers d’études statistiques : les survivants d’Hiroshima ont en effet montré des pathologies cardiaques, respiratoires ou digestives un peu plus fréquentes que dans des populations équivalentes. Ces pathologies sont probablement dues à un vieillissement cellulaire induit par l’irradiation brutale reçue lors de l’explosion.
Il est clair que l’utilisation des grays n’est pas bien adaptée à l’évaluation des effets biologiques, et des risques encourus par une irradiation. La Commission internationale de protection radiologique (CIPR en anglais) a donc proposé de pondérer la dose reçue (mesurée en grays) par des coefficients qui tiennent compte de la nature du rayonnement et de la cible touchée. C’est ainsi qu’a été défini le sievert (Sv), ainsi nommé en l’honneur de Rolf Sievert, pionnier de la radioprotection : la dose reçue, mesurée en grays, est multipliée par un coefficient de pondération Q propre à chaque rayonnement et par un coefficient de pondération N propre à chaque organe humain. Ces coefficients de pondération sont empiriques, ils ont été estimés par la fréquence des cancers des survivants d’Hiroshima, et ils évoluent au fil des recherches. Le sievert a remplacé le rem qui vaut 0.01 Sv.
 Rolf Sievert
Karolinska Institutet Stockholm
Rolf Sievert
Karolinska Institutet Stockholm
Le coefficient Q vaut 1 pour des bêtas, pour des rayons X et pour des gammas. Q varie de 5 à 20 pour des neutrons selon leur énergie, et Q est égal à 20 pour des alphas, dont l’énergie est déposée dans un volume plus petit. Le coefficient N, lui, est fixé à 0.20 pour les organes reproducteurs, à 0.12 pour la moelle osseuse, le côlon, le poumon, l’estomac, à 0.05 pour la vessie, le sein, le foie, l’œsophage, la thyroïde, et à 0.01 pour peau et les os. On peut également estimer empiriquement des coefficients N pour d’autres organismes : les insectes sont 10 à 100 fois plus résistants que les humains aux rayonnements ionisants, d’où l’idée qu’après une guerre nucléaire généralisée, il ne restera sur Terre que les blattes et les fourmis.
Il faut aussi tenir compte de la durée au cours de laquelle une dose est reçue : une dose de 1 Sv reçue en quelques heures peut entraîner (temporairement) des nausées, une baisse des globules blancs mais rarement la mort, et tout finit par revenir à la normale. Les dommages sont plus sérieux au-delà de 2 Sv, ils deviennent irréversibles, et le risque de mortalité augmente avec la dose : 5 Sv entraînent la mort en quelques semaines dans 50% des cas (dose létale 50). La même dose reçue sur plusieurs années n’entraîne pas de manifestation clinique immédiate (mais cela n’exclue pas un risque à plus long terme). Enfin 10 Sv reçus en quelques heures conduisent à des dommages immédiats très sévères entraînant la mort en quelques semaines.
Le sievert est surtout utilisé en radioprotection pour fixer les seuils autorisés car il permet d’additionner les doses reçues au cours du temps et d’estimer le risque d’apparition de cancers dans la population touchée. Le nombre de cancers supplémentaires dans une population semble en effet à peu près proportionnel au nombre de sieverts, et il est de l’ordre de 5% par sievert reçu par an. Autrement dit, parmi 1000 personnes exposées à une dose de 1 Sv, on estime qu’il apparaîtrait, à terme, 50 cancers supplémentaires (à comparer aux quelque 280 cancers attendus sans cette irradiation).
La relation linéaire entre irradiation et augmentation du nombre de cancers semble bien vérifiée au-delà de 100 mSv, mais aucune étude épidémiologique n’indique d’augmentation significative du nombre de cancers dans les populations recevant moins de 50 mSv par an (qui est d’ailleurs la radioactivité naturelle dans certains villes sur Terre). Savoir s’il est légitime de l’extrapoler pour des doses beaucoup plus faibles ou s’il existe un seuil en dessous duquel elle perd sa valeur est l’objet de discussions parfois violentes. Certains défendent l’idée qu’une faible dose d’irradiation serait même bénéfique (hormesis).
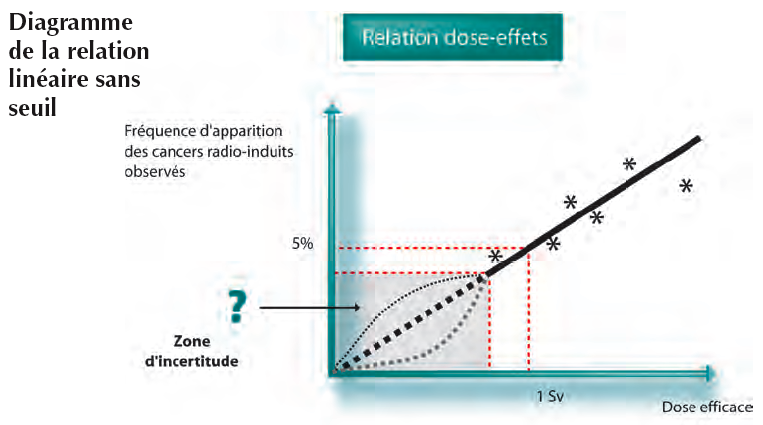
Relation linéaire sans seuil entre l’irradiation reçue et l’augmentation de la fréquence des cancers ASN
La complexité des mécanismes conduisant d’une irradiation à une carcinogenèse rendent la question difficile, et les études épidémiologiques ne sont pas utilisables. La relation linéaire sans seuil extrapolée aux faibles doses implique par exemple qu’il y aura aussi bien 50 cancers supplémentaires parmi mille personnes recevant 1 Sv, que parmi un million recevant 1 mSv. Mais ces 50 cancers sont repérables parmi 280, mais pas du tout parmi 280 000. Malgré de nombreuses réticences, la relation linéaire sans seuil est utilisée par la plupart des organismes nationaux et internationaux en application du « principe de précaution ». Depuis 1900, la norme administrative a réduit de 5 à 1 mSv/an le seuil autorisé de dose dépassant la radioactivité naturelle et médicale (et de 50 à 20 mSv/an pour les professionnels). C’est le millième de la dose qui augmente de 5% le risque de cancer chez l’adulte. Pour fixer les idées, précisons que la radioactivité ambiante que nous absorbons chaque année se situe entre 3 et 4 mSv en France (avec d’importantes variationsindividuelles). Le tiers de cette dose vient des applications médicales, une radiographie pulmonaire délivrant de 0.02 à 0.1 mSv, un scanner du crâne de 1 à 10 mSv.
Lente prise de conscience des dangers
La toxicité des rayons X conduisit Antoine Béclère, le pionnier de la radiologie en France, à préciser dès 1904 les « Moyens de protection des médecins et de leurs patients contre l’action nocive des nouvelles radiations ». Gants, tabliers, protections de plomb commencèrent à faire leur apparition, mais peu de gens les utilisèrent au début.

Antoine Béclère (1856-1939), pionnier de la radiologie en France
William Herbert Rollins, dentiste à Boston, mena de 1896 à 1904 de nombreuses expériences sur le matériel de radiologie (tubes, collimateurs, protections), il montra que les rayons X pouvaient tuer le fœtus d’un cobaye (l’animal !) et il recommanda donc d’éviter les radiographies pelviennes des femmes enceintes. En 1906 fut formulée la loi de Bergognié et Tribondeau, pionniers de la radiobiologie : les rayons X agissent avec d’autant plus d’intensité sur les cellules que l’activité reproductrice de ces cellules est grande, et que leur morphologie et leurs fonctions sont moins définitivement fixées. La principale difficulté rencontrée, en dehors de la méconnaissance des mécanismes biologiques mis en œuvre, était le manque de moyens de mesure de l’énergie et du flux de ces rayons : la calibration de l’appareil consistait à mesurer le temps d’apparition d’une rougeur sur la main d’un cobaye (le radiologue, cette fois !). Il fallait une vingtaine de minutes pour cela et la dose reçue était alors de 5 à 6 grays, de quoi faire frémir tout radiologue contemporain (c’est à peu près la dose utilisée pour irradier un cancer du sein). Le gray correspond à l’absorption d’une énergie d’un joule par kilo de tissu. Pour tenir compte de la différence d’effet biologique selon la nature du rayonnement et celle de la cellule, on a défini le sievert : un sievert correspond à un gray multiplié par des coefficients de pondération. La première norme, en 1902, correspondait à 0.1 gray par jour (30 grays par an). Elle n’était pas fixée par ses effets biologiques mais par la sensibilité du détecteur : une plaque photographique qui se voilait progressivement.
Les dangers du radium se sont également très vite manifestés. Giesel et Walkoff avaient relaté dès 1900 la brûlure sur leur bras due au contact pendant quelques heures d’un sel de radium faiblement actif. Les 3 et 4 avril 1901, Henri Becquerel emporta à une conférence un petit tube de sel de radium fortement actif prêté par Pierre Curie. Il le plaça dans son gilet et une forte rougeur apparut suivie d’une plaie suppurante. Pierre Curie reproduisit sur lui-même l’expérience de Giesel et il raconta par le menu l’évolution de la plaie dans une note à l’Académie des Sciences, « Action physiologique des rayons du radium », cosignée par Becquerel. Il signalait que Marie Curie avait elle aussi été brûlée et que leurs doigts desquamaient. La santé de Pierre Curie se détériorait d’ailleurs gravement, il était très fatigué, il avait d’intenses douleurs osseuses et il perdait facilement l’équilibre. Ces troubles étaient attribués au surmenage et à leurs difficiles conditions de travail, mais leur laboratoire était fortement contaminé : Marie Curie raconta plus tard que « L'une de nos joies était d'entrer la nuit dans notre atelier. Nous percevions de tous côtés les silhouettes lumineuses des flacons et des capsules qui contenaient ces produits. » Leurs carnets de notes furent décontaminés avant d’entrer à la Bibliothèque nationale, de nombreuses années plus tard, ainsi que le bureau et le laboratoire de Marie Curie à l’Institut du Radium (aujourd’hui musée Curie à Paris). Il est difficile d’estimer la quantité de rayonnement reçue par les Curie et leurs assistants, comme par tous les pionniers de la radioactivité, mais elle tournait probablement autour de 1 Sv/an (soit 300 fois la radioactivité naturelle).


Une page des carnets de laboratoire des Curie et son autoradiographie montrant les dépôts de radium dans l’angle supérieur gauche, ainsi qu’une empreinte de pouce en bas à droite. (Musée Curie, Paris)
« J'ai retiré ce radium de la pechblende
Et j'ai brûlé mes doigts à ce feu défendu » Aragon (Les yeux d’Elsa 1942)
Les dangers du radium à forte dose étant bien établis, des doutes naquirent quant à l’innocuité du radium à de plus faibles doses: le cas des Radium girls, puis celui d’Eben Byers, permirent de comprendre que le radium s’accumulait dans les os et y détruisait les cellules de la moelle osseuse. Le danger majeur pour les médecins venait cependant des rayons X, beaucoup plus largement utilisés, et les premières normes de radioprotection datent de 1921 en Grande-Bretagne (X-ray and Radium Protection Committee), de 1922 aux États-Unis (Roentgen Ray Society). G. Pfahler suggéra en 1922 d’utiliser systématiquement des films photographiques pour enregistrer les doses reçues par les opérateurs et Edith Quinby l’imposa dès 1923 au personnel du Memorial Hospital de New York. À partir de ses travaux sur les opérateurs en radiologie, Arthur Mutscheller proposa en 1923 de limiter la dose de rayonnement tolérable à 700 mSv par an : cela correspondait à 1/10 des doses alors reçues par les opérateurs qui ne montraient aucun signe clinique d’irradiation. La même année, Rolf Sievert fit indépendamment une proposition analogue en suivant une démarche similaire (1/100 de la dose provoquant un érythème par mois). Il était alors extrêmement difficile de mesurer les doses de rayonnement émises par les appareils, et plus encore les doses reçues par les opérateurs et par les patients. Des décennies de tâtonnements furent nécessaires avant que soient mis au point et généralisés des compteurs simples et fiables. Mais c’était une étape indispensable pour pouvoir quantifier la relation entre irradiation et risque. Quantifier le risque n’était pas simple non plus dans la mesure où aux effets déterministes immédiats s’ajoutaient des effets stochastiques à long terme.

Une stèle fut érigée en 1935 à la mémoire de 350 physiciens et radiologues victimes des rayons X et de la radioactivité
Le généticien Hermann Joseph Muller, voulant accélérer les mutations chez les drosophiles (mouches du vinaigre) eut l’idée de les irradier avec des rayons X. Ses mesures quantitatives des taux de mutation en fonction de l’intensité du rayonnement firent la une des media en 1927 et elles déclenchèrent de très nombreux travaux sur les effets génétiques des rayonnements, en particulier chez l’homme. Il reçut le prix Nobel de médecine en 1946 « Pour la découverte de la production des mutations par les rayons X ». On vérifia très vite que les effets mutagènes ne se limitaient pas aux rayons X, mais s’étendaient aux rayons alpha, bêta et gamma. Les effets biologiques des rayonnements étaient d’ailleurs très étudiés, en particulier la possibilité qu’ils stimulent la croissance des végétaux. Par exemple Gioacchino Failla collabora avec le botaniste P.S. Henshaw en 1931 à une étude de l’efficacité comparée des rayons X et des rayons gamma (les uns et les autres sont des rayonnements électromagnétiques, mais d’énergie différente).

Le généticien H.J. Muller qui démontra que les rayonnements ionisants provoquaient des mutations
Commissions
En 1928, lors du Congrès international de radiologie, fut créée une commission (International X-ray and Radium Protection Committe) chargée d’établir des limites d’exposition du personnel médical aux sources de rayonnements ionisants. Ce fut l’ancêtre de l’actuelle Commission internationale de radioprotection (CIPR), organisation non gouvernementale sans but lucratif, toujours liée à la Société internationale de radiologie. Dans un premier temps, l’attention se porta sur les effets déterministes afin d’établir une limite en dessous de laquelle aucun effet ne semblait repérable. Cette limite fut placée autour d’un sievert par an. Puis la discussion se déplaça vers les effets indirects, en particulier ceux qui sont liés au cumul de doses comme le drame des Radium girls l’indiquait, pour définir un seuil de tolérance. Une des premières recommandations apparut en 1934, sous la forme d’une dose tolérable d’un milligray par jour. Cette norme portait sur un débit de dose, l’idée étant qu’il existe un seuil en dessous duquel l’organisme corrige complètement les dommages causés aux cellules. Il était cependant évident que la même dose causait des dommages différents selon les régions du corps touchées, et l’on doit à Failla l’idée de moduler la dose tolérable selon la région du corps : il proposa en 1932 de placer un plafond de 1 mSv/jour pour le corps, mais de 5 mSv pour les mains (le sievert, comme le gray, sont des doses par unité de masse).
La radioprotection avait cependant des progrès à faire dans les laboratoires de physique nucléaire, ainsi que dans les services de médecine nucléaire. Jusqu’à sa mort en 1934, Marie Curie eut beaucoup de mal à accepter que le radium puisse être la cause des troubles de santé qui la minaient. « J’ai deux enfants, mais la radioactivité est aussi mon enfant » disait-elle. Il était encore fréquent à l’Institut du Radium d’utiliser des pipettes pour aspirer des liquides radioactifs. Pourtant, à Berlin, Lise Meitner avait isolé par du plomb certaines salles de son laboratoire de l’Institut Kaiser Wilhelm, installé des hottes aspirantes, imposé le lavage fréquent des mains, et bien sûr les produits radioactifs étaient stockés dans des boîtes de plomb et manipulés avec des pinces.
En 1935 Louis Harold Gray (qui fut l’élève de Rutherford et de Chadwick à Cambridge) reprit des idées formulées en 1912 par Lawrence Bragg sur l’interaction des rayons gamma avec la matière et développa le principe (de Bragg-Gray) de mesure de l’énergie des rayons gamma et de leur dépôt dans la matière. Il s’intéressa aussi aux effets biologiques des neutrons et il construisit un générateur de neutrons lui permettant de rassembler de très nombreuses données fort utiles à la radiothérapie du cancer.

Louis Harold Gray (1905-1965)
Le projet Manhattan marqua un tournant dans la radioprotection. Le responsable de la protection radiologique, Robert Stone, demanda une synthèse de toutes les connaissances sur les risques radiologiques et il définit la règle selon laquelle l’exposition devait demeurer aussi basse que possible (sans jamais, bien entendu, dépasser la dose déterministe tolérable). Il y avait là un changement notable d’optique, avec le passage d’une dose « tolérable » à une dose « admissible ». Ce n’était pas seulement une question de vocabulaire, mais la prise en compte à un haut niveau de responsabilité de l’idée qu’il faut toujours viser la dose de rayonnement la plus faible que l’on puisse raisonnablement atteindre (principe ALARA, As low as reasonably achievable), et ne pas se contenter d’une dose qui ne provoque pas de symptôme visible. Les discussions au cours du demi-siècle qui suivit portèrent en grande partie sur le sens à donner au mot « raisonnablement ».
L’étude clinique de nombreuses personnes exposées au radium permit en 1941 de fixer une nouvelle limite de 0.1 microgramme (0.1 µCi soit 3700 Bq) à la quantité de radium absorbé, les effets délétères apparaissant au-delà d’un microgramme fixé dans les tissus. Cette étude servit en 1944 à fixer à 0.3 µCi la limite de tolérance pour le plutonium (limite ensuite réduite à 0.03 µCi) dans le cadre du projet Manhattan. Celui-ci conduisit également Karl Z. Morgan à présenter en 1945 les premiers calculs de concentrations admissibles (dans le corps et dans l’environnement) pour de nombreux noyaux radioactifs. Une conférence tripartite (USA, Canada, Grande-Bretagne) se tint en 1949 à Chalk River, au Canada, pour rassembler toutes les données disponibles concernant la radioprotection. C’est à la suite de cette conférence que la CIPR publia en juillet 1950 de nouvelles limites de dose : 150 mSv par an (pour la moelle osseuse, 300 pour la peau) pour les professionnels. Et pour la première fois une dose-limite était proposée pour le public, en raison des craintes portant sur les effets génétiques des rayonnements. La limite de 15 mSv par an était dix fois plus basse que pour les professionnels parce que ceux-ci étaient en majorité des adultes en bonne santé suivis médicalement de beaucoup plus près que le reste de la population. La Commission internationale sur les unités radiologiques proposa en 1953 de nouvelles unités remplaçant le röntgen (défini à partir de l’ionisation entraînée par des rayons X) en introduisant la notion de dose absorbée : le rad déposait 100 ergs par gramme de substance absorbante, le rem tenant lui compte de l’impact biologique. Le passage du système CGS au système MKSA conduisit à remplacer en 1975 le rad par le gray (100 rad = 1 gray) et le rem par le sievert (100 rem = 1 sievert).
L’essai de la première bombe H à Bikini en 1954, et l’irradiation accidentelle d’un thonier japonais par ses retombées, souleva de vives inquiétudes sur les effets des retombées des explosions nucléaires. Il apparut que tout le monde était concerné par les rayonnements ionisants, pas seulement les radiologues ou les travailleurs du nucléaire (essentiellement militaire à cette époque). L’ONU créa alors en 1955 l’UNSCEAR (United nations scientific committee on the effects of atomic radiations) chargé « d’évaluer les niveaux et les effets des rayonnements ionisants au niveau mondial et de fournir une base scientifique pour la radioprotection ». L’UNSCEAR joue aujourd’huiun rôle central dans l’évaluation et la limitation des risques liés aux rayonnements ionisants, en liaison évidemment avec la CIPR, l’Organisation mondiale de la santé (OMS) et l’Agence internationale de l'énergie atomique (AIEA).


Schéma de principe et photo d’un film photographique servant à mesurer par son noircissement la dose totale de rayonnement reçue. Certaines parties du film sont masquées par une plaque d’aluminium, de cuivre, de plomb ou de plastique servant de filtres pour mieux préciser la dose (précis au-delà d’un millisievert). La quantité de rayonnement reçue n’est cependant connue qu’après le développement du film. © BBC
La CIPR abaissa en 1957 la limite de dose recommandée de 150 à 50 mSv/an pour les professionnels et de 15 à 5 mSv/an pour le public. Les conséquences génétiques des rayonnements semblaient avoir été surestimées, mais par contre le risque de cancers semblait, lui, avoir été sous-évalué au vu du nombre de leucémies apparues chez les survivants d’Hiroshima, puis de cancers solides (dont le temps de latence est plus grand que celui des leucémies). Ce risque conduisit à abaisser la limite dans l’idée qu’une dose faible pouvait causer autant de cancers dans une population étendue qu’une dose importante sur une population réduite (principe de la relation linéaire sans seuil). L’accent mis initialement en radioprotection sur la réduction des effets déterministes se portait donc de plus en plus vers la réduction des risques statistiques. La CIPR insista en 1959 pour « maintenir les doses d’exposition aussi bas qu’il est praticable et d’éviter toute exposition inutile », ce qui impliquait d’ailleurs qu’il existait des expositions utiles. Cette formulation évolua quelque peu au fil des années, devenant par exemple en 1977 « aussi bas que raisonnablement possible compte tenu des dimensions économiques et sociales ». Ce passage du champ médical et sanitaire au champ économique, social et politique reconnaît qu’il n’existe pas de risque zéro, et que c’est au politique de déterminer le degré de risque accepté en regard des avantages que la société peut en tirer. Ceci est évidemment très loin d’être limité à la seule radioprotection ! Toute activité présente en effet un risque, et nous évaluons continuellement le risque que nous prenons face à l’intérêt que nous trouvons à poursuivre cette activité. La difficulté est évidemment dans la pertinence de l’évaluation que nous faisons…

Dosimètre électronique individuel, permettant de mesurer en temps réel la dose de rayonnement X et gamma reçue (en microsieverts), et par mémorisation la dose totale reçue (jusqu’à 10 ou 100 mSv selon les modèles) au cours d’une période donnée. D’autres modèles détectent les neutrons, les alpha ou les bêta. © Aloka
La CIPR baissa à nouveau la limite en 1990 de 50 à 20 mSv/an pour les professionnels et de 5 à 1 mSv/an pour le public à la suite d’un réexamen des doses de rayonnement reçues par les survivants d’Hiroshima. Un nouveau calcul de la proportion de rayons gamma et de neutrons dans le rayonnement émis par l’explosion, et la découverte que de nombreux survivants se trouvaient en réalité plus loin de l’explosion qu’ils ne l’avaient déclaré (leur indemnisation augmentait avec la proximité du centre de l’explosion), ont conduit à estimer qu’ils avaient reçu en réalité des doses plus faibles qu’on l’avait supposé. Ces changements sont d’ailleurs loin de faire l’unanimité, de nombreux spécialistes de médecine nucléaire et de radioprotection estimant que l’abaissement des seuils ne repose pas sur des bases médicales sérieuses, tandis qu’inversement d’autres partent du principe que toute dose, aussi faible soit-elle, est dangereuse et mettent en cause l’indépendance des membres de la CIPR (radiobiologistes et experts en radioprotection), et de ceux de l’OMS, de l’UNSCEAR et de l’AIEA. La CIPR a publié en 2007 de nouvelles recommandations, qui reprennent largement celles de 1990, et rappellent que la radioprotection repose aujourd’hui sur trois principes:
- Optimiser toute exposition pour qu’elle soit aussi basse que raisonnablement possible (principe ALARA)
- Justifier toute exposition aux rayonnements ionisants (par exemple pour une radiographie)
- Limiter les doses en dessous des seuils réglementaires

Évolution au cours du temps des doses tolérées en radioprotection (échelle verticale logarithmique, 100 millirem= 1 mSv) © Alamos National Laboratory
Pour tout savoir -ou presque- sur la radioprotection:
