Alain Bouquet - L'électron
Attention: ces pages ne sont plus mises à jour car le site a déménagé. Il se trouve désormais à: Pensez à mettre à jour vos signets et bookmarks! |
Champs, Noyaux & particules
Radioactivité
Noyaux, protons et neutrons
- Noyau atomique: Rutherford
- Noyau atomique: Bohr, Soddy et Moseley
- Noyau atomique: Aston et Rutherford
- Neutron: Chadwick
- Neutron: Joliot-Curie
- Neutron: Fermi
Intruments, accélérateurs et détecteurs
Mécanique quantique
- Mécanique ondulatoire
- Formalisme quantique
- Applications
- Théorie quantique des champs
- Électrodynamique quantique
Fission nucléaire
Fusion nucléaire
Particules en tout genre
rayons cathodiques
Électricité
Les rayons cathodiques furent un sujet d’étude qui passonna les physiciens, certains d'entre eux en tout cas, tout au long du 19° siècle. Le point de départ est, encore, Faraday et ses recherches sur la nature de l'électricité. Une des questions ouvertes était de savoir si l'électricité était un fluide (continu) ou un courant de particules (discrètes). Ce dernier point de vue fut en particulier avancé par Fechner en 1845 puis Weber en 1848, influencés par les travaux de Faraday sur l'électrolyse dans laquelle l'électricité était portée par des ions de charge donnée. Ces travaux de Faraday en 1833 (synthétisés dan sun traité en 1839) établissaient des lois:
- la quantité de matière déposée aux électrodes est proportionnelle à la quantité d'électricité qui a circulé;
- les équivalents électrochimiques des éléments (en unités hydrogène) sont constants d'une réaction à une autre (ce qui n'est pas exact, ils sont proportionnels à la valence, notion développée bien plus tard, par Kekulé entre autres, et helmholtz corrigea Faraday sur ce point en 1881)
Faraday était partisan de la réalité physique des atomes, et donc de l'existence de charges électriques élémentaires portées par les ions. Les atomes n'avaient pas de structure interne pour Faraday, mais qu'étaient alors les ions? S'ils n'étaient pas des fragments d'atomes brisés, était-ce un effet dynamique, une sorte de polarisation des atomes? La situation était très confuse. Maxwell jugeait nécessaire une structure interne des atomes pour expliquer les spectres de raies qu'il attribuait à des rotations et des vibrations internes aux atomes (plus de six degrés de liberté lui semblaient requis). D'un autre côté la stabilité des atomes au travers de toutes les réactions chimiques était difficile à admettre s'ils avaient une structure interne.
Les rayons cathodiques
Parmi les corps conducteurs de l'électricité et les corps isolants qui ne la conduisaient pas, les gaz étaient un cas intéressant: un espace entre conducteurs interrompait la passage du courant, ils étaient donc isolants, mais si la tension était assez forte, une brève étincelle jaillissait entre les deux conducteurs et permettait le passage du courant. Watson avait noté dès 1752 que si la décharge se faisait dans un gaz raréfié, ce gaz devenait brièvement lumineux à côté de l'étincelle.

En 1838, Faraday étudiait la formation d'étincelles entre deux électrodes soumises à une forte tension. Il eut l'idée de placer les électrodes à l'intérieur d'une ampoule dans laquelle il pouvait changer la nature du gaz et varier sa pression. En baissant la pression (en faisant un vide partiel), Faraday remarqua que la conduction était améliorée (effectivement l'absorption des électrons du courant par le gaz, responsable du caractère isolant, diminue quand le nombre d'atomes absorbants diminue) et que l'ampoule devenait faiblement lumineuse. S'agissait-il d'un quatrième état de la matière, après l'état solide, liquide et gazeux? Cette lumière provient en fait de la désexcitation des atomes du gaz. Farady remarqua également un espace sombre près le la cathode (lespace de Faraday).

Le montage de Faraday (faiblement étanche en raison du bouchon de liège que traversaient les électrodes)
L'expérience fut souvent répétée en variant
- la tension du courant
- la nature du gaz (ou de la vapeur de mercure, de sodium…), ce qui changeait la couleur de la lumière émise
- sa pression
Phénomène fascinant, mais inexpliqué: la lumière émise par le gaz était très différente de la lumière émise par la Soleil ou par une bougie car, observée à travers un spectroscope, elle ne montrait pas un spectre continu mais seulement quelques raies isolées. Ces raies étaient caractéristiques du gaz (ne dépendant ni de la tension électrique, ni de la pression ni de la température). Gustav Kirchhoff (1824-1887) établit qu'un objet chaud émet un spectre continu qui ne dépend pas de la nature de l'objet mais uniquement de sa température, tandis qu'un gaz élecriquement excité émet un spectre formé de raies qui ne dépend pas de la température du gaz mais uniquement de sa nature.
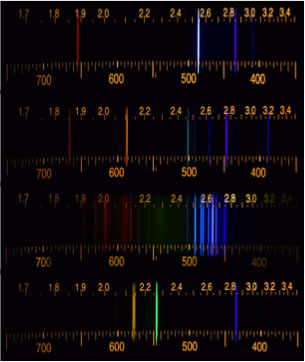
Spectres de raies pour l'hydrogène, l'hélium, le krypton et la vapeur de mercure
En 1855, Heinrich Geissler mit au point une pompe à vide utilisant le mercure, capable de diminuer la pression jusqu'à 100 pascals (soit 10-3 atm) puis 10 Pa. En 1857, Geissler parvint également à souder des électrodes à l'intérieur d'un tube de verre dans lequel il avait fait le vide. Parce qu'on pouvait leur donner presque toutes les formes et toutes les couleurs, les tubes de Geissler eurent un immense succès commercial, jusqu'à la mise au point des "tubes au néon".
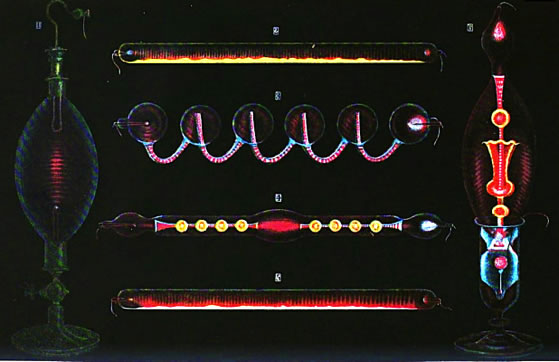
La luminosité augmentait avec la tension, conduisant à la recherche de tensions de plus en plus élevées. Les piles, même montées en série, de délivraient que quelques dizaines de volts, mais la mise au point de la bobine d’induction par Ruhmkorff en 1851 permit d'atteindre des tensions de plusieurs kilovolts (kV).
Julius Plücker (1858) enseignait à l'université de Bonn, à proximité immédiate de l'atelier de Geissler, et il effectua avec ces tubes toute une série de travaux dans les années 1857-1860, examinant la taille de la région lumineuse selon la pression, la tension ou le gaz. Il observa également, en diminuant la pression jusqu'à quelques pascals (1 Pa=10-5 atm) que la luminosité diminuait et que le tube devenait sombre, mais qu'une lueur résiduelle apparaissait près de l'anode: le verre devenait fluorescent et Plücker montra que la tache fluorescente changeait de forme en approchant un aimant.
Son élève Johann Hittorf montra en 1859, en interposant des obstacles entre cathode et anode, que ces obstacles découpaient une ombre nette près de l'anode. Il en conclut que des rayons (=rectilignes) partaient de la cathode en direction de l'anode, et que les obstacles les arrêtaient. D'où le terme de "rayons cathodiques" donné en 1876 par Goldstein, qui confirma les résultats de Hittorf. Goldstein pensa un temps que ces rayons étaient des particules chargées avant de changer d'avis en 1880 et de soutenir l'idée qu'il s'agissait de rayonnements électromagnétiques.


Le véritable auteur de ces notes est démasqué
Les expériences sur les décharges électriques dans les gaz étaient très compliquées à interpréter, en particulier en raison de nombreux effets secondaires souvent incontrôlés, dus au gaz résiduel, au verre, aux électrodes, etc. Ces effets diminuaient quand la pression baissait, d'où un effort continu pour baisser la pression, et augmenter la tension. Sir William Crookes améliora beaucoup le tube de Geissler en 1869 (1879?):
- cathode concave (focalisation)
- anode décalée
- tensions plus fortes (jusqu’à 100 kV grâce à une bobine de Ruhmkorff)
- et surtout pression < 0,1 Pa (10-6 atm) grâce aux progrès dans les pompes à vide

Un tube de Crookes typique mesurait 30 cm de long et 2 cm de diamètre, avec divers renflements et extensions selon le but recherché. Son tube se diffusa dans tous les laboratoires (= Allemagne, Royaume-Uni et France) et donc « tout le monde » étudia les rayons cathodiques pour en élucider la nature. Celle-ci restait mystérieuse. Crookes suggéra en 1878 qu'il s'agissait sans doute de corpuscules porteurs d'une charge électrique, et les identifia aux ions du gaz. Il évoquait de la "matière radiante", des "torrents moléculaire" et un "quatrième état de la matière". Crookes plaça un petit moulin (radiomètre de Crookes) sur le trajet des rayons qui le faisaient tourner: ils transportaient donc une énergie et une impulsion. Une feuille d'étain placée sur le trajet chauffait.
En 1883, Heinrich Hertz n'observa aucune déviation des rayons cathodiques par un champ électrique, et il en conclut qu'il devait plutôt s'agir d'une onde électromagnétique, et que les courants de matière étaient des effets parasites. Il confirma son interprétation en 1891 en montrant que ces rayons pouvaient traverser de minces feuilles métalliques. Son élève Lenard eut alors l'idée de réaliser des tubes dans lesquels une ouverture dans le verre (fenêtre) était fermée par une feuille métallique opaque à la lumière mais laissant sortir les rayons cathodiques, pour étudier leurs effets à l'extérieur du tube.
Cependant, Thomson montra en 1894 que la vitesse des rayons cathodiques était inférieure à la vitesse de la lumière, et Jean Perrin collecta en 1895 les rayons cathodiques dans un cylindre métallique et il montra ainsi qu'ils déposaient des charges électriques. Il ne pouvait donc pas s'agir d'ondes électromagnétiques. Une controverse divisa alors l'école allemande (pour qui les rayons cathodiques sont des ondes électromagnétiques) et l'école franco-britannique (pour laquelle il s'agissait de corpuscules).
L'idée de corpuscules chargés électriquement fut renforcée en 1896 par une découverte faite dans un tout autre domaine. Cette année-là, Pieter P. Zeeman découvrit que les raies spectrales émises par le gaz s'élargissaient en présence d'un champ magnétique, cette largeur augmentant avec l'intensité du champ (effet Zeeman). En réalité le champ magnétique n'élargit pas une raie mais la scinde en plusieurs composantes, dont l'écart est proportionnel au champ magnétique, mais la résolution des spectroscopes était alors insuffisante pour résoudre ces composantes. Zeeman ne put d'ailleurs découvrir l'effet qui porte son nom que grâce à la réalisation peu avant par Rowland de réseaux de diffraction portant 400 puis 800 lignes par millimètre (équidistantes à mieux de 1/4000 mm). Hendrik Antoon Lorentz expliqua aussitôt cet effet en supposant que la lumière était émise par des particules chargées accélérées dans l'atome et il en déduisit un rapport masse/charge électrique de ces particules intra-atomiques: q/m ~ 1011 C/kg.
Parenthèse: le calcul fait par Lorentz en 1896.
En 1892, Lorentz s'était lancé dans une réinterprétation des équations de Maxwell en termes de charges électriques et de courants de charges. Le vocabulaire étant encore peu fixé, Lorentz parlait de particules en 1892, d'ions en 1895 et d'électrons en 1899. C'est ainsi qu'il explicita en 1895 la "force de Lorentz" F = q(E+VxB) s'exerçant sur une charge q de vitesse V, soumise à un champ électrique E et un champ magnétique B. En ce cas, une particule de masse m placée dans un champ magnétique B uniforme suit une trajectoire circulaire (plus généralement une hélice dans la direction du champ) avec une fréquence (dite fréquence de Larmor) fLarmor qui ne dépend que du champ B et du rapport q/m mais non de la particule elle-même, de sa vitesse ou des autres forces qu'elle pourrait subir. Si cette particule est par ailleurs naturellement en rotation à la fréquence fatome (par exemple parce qu'elle oscille dans un atome à cette fréquence, par quelque mécanisme que ce soit), le mouvement résultant est la superposition de trois mouvements périodiques dont les fréquences sont fatome , fatome + fLarmor et fatome – fLarmor . Lorentz supposa simplement que la largeur (apparente) de la raie était le double de la fréquence de Larmor, ce qui lui donna la valeur du rapport q/m de "ce qui transporte l'électricité dans un atome".
Le rapport masse/charge électrique obtenu par Lorentz, de trois ordres de grandeur plus faible que celui de l'ion le plus léger H+, ne semble avoir étonné ni Lorentz ni Zeeman. Celui-ci observa en 1897 une séparation des raies du cadmium (à 480 nm), et non un simple élargissement, et une polarisation de la lumière dont le sens lui indiqua que la charge était négative. Zeeman et Lorentz partagèrent en 1902 le prix Nobel de physique.
Les travaux sur les rayons cathodiques furent mis en veilleuse en 1896, tous les experts du domaine se focalisant sur les rayosn X nouvellement découverts, avant de revenir (certains du moins) aux rayons cathodiques en 1897 pour le sprint final.
Ce qui se passe physiquement
La passage inévitable dans le gaz résiduel du tube (de Faraday, Geissler ou Crookes) de rayons cosmiques ou de la radioactivité naturelle ionise partiellement le gaz. En appliquant une forte tension entre le sélectodes, les ions sont mis en mouvment par le champ électrique ainsi créé et ils entrent en collision avec les atomes du gaz et leurs arrachent des électrons. La suite dépend de la pression du gaz.
Pour une pression "élevée", supérieure à 100 Pa, ces électrons sont vite absorbés par les atomes du gaz. Ceux-ci sont dans un état excité à la suite de cet apport d'énergie, et ils se désexcitent en émettant de la lumière, aux longueurs d'onde caractéristiques du gaz car l'énergie des photons est égale à la différence entre deux niveaux d'énergie de l'atome.
Pour une pression "basse", inférieure à 100 Pa, les électrons vont directement vers l'anode, mais ils ne forment qu'une faible partie des rayons cathodiques. Ceux-ci proviennent pour l'essentiel des ions qui, accélérés vers la cathode, entrent en collision avec elle et lui arrachent des électrons qui, repoussés par la cathode et attirés par l'anode forment les rayons cathodiques. Le tube est sombre car le gaz est trop peu dense pour être excité et émettre de la lumière, sauf près de l'anode où les électrons frappant le verre du tube et en excitent la fluorescence.
J.J. Thomson
Simultanément, Wiechert, Kaufmann et Thomson parvinrent à mesurer un rapport masse/charge électrique pour les rayons cathodiques, mais c'est Thomson qui eut l'honneur du prix Nobel en 1906 pour la découverte de l'électron, sans doute parce qu'il fut le seul (avec Wiechert) à en déduire qu'il s'agissait d'une particule très légère, et qu'il en mesura séparément la charge en 1899.
Emil Wiechert (1861-1928) avait supposé (correctement) dès 1896 que les rayons X étaient des rayonnements électromagnétique de très courte longueur d'onde. En 1897 il était parvenu à dévier des rayons cathodiques par un champ magnétique et à en estimer par ailleurs la vitesse par une mesure du temps de transit. Il avait déduit des ces observation une valeur du rapport masse/charge et en supposant que la charge était la charge élémentaire de Stoney, que les rayons cathodiques étaient des flux de particules 2000 à 4000 fois plus légères que l'atome d'hydrogène. Il présenta ces résultats lors de séminaires à Königsberg (où il était professeur-assistant à l'université) puis il rejoignit peu après l'université de Göttingen où se tourna avec un grand succès vers la géophysique, et sa contribution à l'étude des rayons cathodiques tomba dans l'oubli.
Walter Kaufmann (1871-1947) mesura lui aussi le rapport masse/charge par la courbure magnétique des rayons cathodiques et montra que ce rapport ne dépendait pas du gaz résiduel. Il ne pouvait donc pas s'agir des ions du gaz. L'idée de particules était peu en vogue à Berlin, où travaillait alors Kaufmann et celui-ci n'alla pas plus loin. Il se rendit célèbre une dizaine d'années plus tard par ses mesures de la "masse relativiste" de l'électron, qui semblaient réfuter la théorie de la relativité resteinte d'Einstein et confirmer la théorie de l'électron présentée en 1902 par Max Abraham (1875-1922).
Au laboratoire Cavendish, Joseph John Thomson n'avait pas abandonné l'étude des rayons cathodiques, même s'il avait lancé plusieurs de ses élèves sur les rayons X. Il pensa que si Hertz n'avait pas réussi à dévier les rayons cathodiques ni avec un champ électrique ni avec un champ magnétique, c'était peut être dû à l'insuffisance de ces champs pour des corpuscules très rapides.
Déviation d'une charge par un champ électrique ou magnétique
Un champ électrique E engendre une force de Coulomb FCoulomb = qE sur une charge électrique q. Si cette charge est celle d'un corpuscule de masse m, celui-ci est soumis à une accélération γ = q/m E. Si le champ est perpendiculaire à la vitesse initiale, l'accélération est constante et transversale et le corpuscule suit une trajectoire parabolique aussi longtemps qu'il est soumis au champ, puis une trajectoire rectiligne dès qu'il n'y est plus soumis. Un peu de géométrie montre que son angle de déviation est θ~ q/m E/V2 où V est la vitesse initiale (inconnue) du corpuscule.

L'expérience de Thomson
Thomson décida de créer un champ électrique intense en plaçant à l'intérieur du tube, dans un vide très poussé, les deux électrodes qui le créaient. Distantes de 1.5 cm, les deux plaques de 5 cm de long étaient soumises à une tension de 225 V (fournies par une batterie) → champ E=1.5*104 V/m.

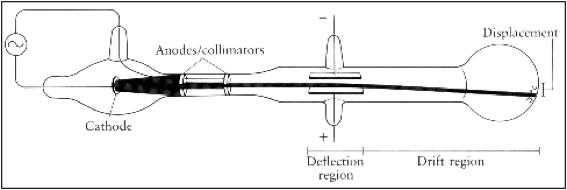
Le tube cathodique de Thomson et le schéma qu’il en donne dans son article. Il mesure près de 2 m de long. Les bagues de collimation (anodes/collimators) servent à s'assurer que les rayons cathodiques ont tous initialement la même direction avant d'entrer dans la zone de déflexion (deflection region), car la cathode les émet un peu dans toutes les directions.
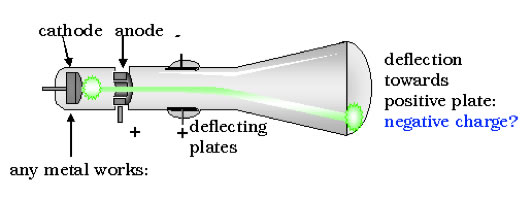
Thomson parvint ainsi à observer un déplacement de quelques centimètres de la tache de fluorescence, démontrant que les rayons cathodiques étaient un flux de corpsucules chargé négativement. Pour obtenir le rapport masse/charge électrique des corpuscules, Thomson avait besoin de connaître leur vitesse. Il eut l'idée d'ajouter un champ magnétique (en plaçant le tube dans l'entrefer d'un aimant).
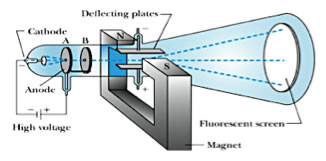
Un champ magnétique B engendre en effet une force de Lorentz FLorentz = q VxB sur une charge q, qui subit donc une accélération γ = q/m V.B qui demeure toujours orthogonale à la vitesse. La charge suit donc une trajectoire circulaire de rayon r = m/q V/B . Ce rayon dépend aussi du rapport masse/charge électrique m/q et de la vitesse initiale V du corpuscule, mais différemment de la déviation électrique. Avec un champ de 5*10-4 T, Thomson obtint un déplacement magnétique de quelques centimètres.

En comparant les effets électrique et magnétique (le mieux est d'ailleurs de compenser une déviation par l'autre, car tous les rayons cathodiques n'ont pas la même vitesse initiale V), Thomson put mesurer séparément la vitesse V et le rapport q/m. Le choix des matériaux employés pour la cathode (aluminium, platine) ou pour le gaz résiduel (air, hydrogène, dioxyde de carbone) n'avait pas d'influence sur le déplacement de la tache de fluorescence, ce qui signifiait qu'il avait affaire à un seul type de corpuscule (en particulier il ne s'agissait pas des ions du gaz employé ou de fragments du métal de la cathode).
Thomson lui-même ne parla que de corpuscules jusqu’en 1913 (le terme électron est dû à Stoney). Il précise dans son article: "We have in the cathode rays matter in a new state, a state in which the subdivision of matter is carried very much farther than in the ordinary gaseous state: a state in which all matter-that is, matter derived from different sources such as hydrogen, oxygen, etc.-is of one and the same kind; this matter being the substance from which the chemical elements are built up." (J.J. Thomson, "Cathode Rays," Philosophical Magazine 44-295, 1897).

Il trouva que les vitesses oscillaient entre 2*107 et 3*107 m/s (1/10 de la vitesse de la lumière) et, pour le rapport q/m, il obtint des valeurs s'étageant entre 6*1010 et 10*1010 C/kg. C'était une très petite valeur (quoiqu'il y paraisse à cause des unités employées) correspondant au millième du rapport q/m du plus léger de tous les ions, celui de l'hydrogène. La valeur actuel du rapport q/m de l'électron est 17.588*1010 C/kg, soit à peu près le double de ce que Thomson avait obtenu. Ce dernier n'avait pas la réputation d'un expérimentateur très talentueux, et il a probablement commis une erreur systématique.
Il utilisa d'ailleurs, toujours en 1897 une méthode différente pour estimer le rapport q/m. Il collecta les rayons cathodiques dans un calorimètre pour mesurer d'une part l'élévation de température (donc l'énergie cinétique NmV2/2) et d'autre part la charge électrique Nq. Il mesura ainsi une charge de 10-5 C/s et une énergie déposée de 10-2 J/s (conduisant à une élévation de température de plusieurs degrés par seconde avec son dispositif), obtenant ainsi une valeur q/m = 20*1010 C/kg, nettement plus proche de la valeur actuelle. Vérifier les calculs.
La charge électrique
Thomson se lança ensuite dans la mesure directe de la charge électrique de l'électron. L'idée d'une charge électrique élémentaire était déjà ancienne, ramontant aux travaux de Faraday sur l'électrolyse. En 1874, lors d'une conférence (publiée en 1881) George Stoney proposa l'existence d'une charge électrique élémentaire, portée en nombre entier d'exemplaire par les ions, et dont il estima la valeur en divisant simplement le faraday, la quantité d'électricité déposant une mole (d'argent par exemple) par le nombre d'Avogadro (nombre d'atomes dans une mole):
e = F/NA
Des estimations du nombre d'Avogadro avaient été données par Loschmidt en 1866 (NA~5*1022), Maxwell (NA~4*1023) et Stoney lui-même en 1868 (NA~1025).
En 1881, Helmoltz défendit l'idée "d'atomes d'électricité" auxquels Stoney donna en 1891 le nom d'électrons. En 1901, Planck donna, à partir du spectre du coprs noir (la distribution de Planck) une estimation de la valeur de la constante k de Boltzmann d'où il déduisit une valeur du nombre d'Avogadro (à partir de la constante R=NAk des gaz parfaits) et enfin une excellente valeur de la charge électrique élémentaire e (sous-estimée de 2%, et ainsi bien meilleure que celle donnée par Thomson en 1899 et même Millikan en 1915).
Thomson mesura la charge des électrons par une méthode de gouttelettes (ancêtre de la méthode de Milikan) avec deux collaborateurs, J.S.E. Townsend et H.A. Wilson.

L'idée était de mesurer la vitesse de chute de goutelettes d'eau, formées autour d'ions dans une chambre de Wilson (mais Charles Thomson Rees Wilson, pas H.A. Wilson). C.T.R. Wilson avait développé cette chambre, précisément au laboratoire Cavendish, dans laquelle de la vapeur d'eau sursaturée était brusquement détendue par le mouvement d'un piston, pour étudier la formation du brouillard. La vapeur instable se condensait en formant des gouttelettes autour des impuretés présentes, grains de poussière ou ions créés par la radioactivité et les rayons cosmiques (alors inconnus d'ailleurs). La chambre de Wilson fut pendant 50 ans l'un des principaux outils de la physique nucléaire et d ela physique de sparticules, permettant de matérialiser la trajectoire des particules, de les identifier et de mesurer leur énergie.
Mais ici, il s'agissait de mesurer la vitesse de chute de ces gouttelettes, qui tendait vers une vitesse limite du fait de la résistance de l'air. Cette vitesse limite correspondait à l'équilibre entre le poids de la goutelette (fonction du rayon de la goutte et de la densité de l'eau) et le frottement de l'air (dépendant du rayon de la goutte et de sa vitesse comme Stokes l'avait montré en 1851). Townsend commença dès 1897 à mesurer ces vitesses limite, et en déduire la masse de chacune des gouttelettes. Puisil mesura la masse totale des gouttelettes recueillies dans un bain d'acide ainsi que la charge électrique totale recueillie dans ce bain. Il obtint ainsi le rapport q/m moyen qu'il ne lui restait qu'à multiplier par la masse de chaque gouttelette pour en obtenir la charge électrique. Il ne lui restait qu'à examiner la distribution de ces charges pour vérifier qu'elle étaient toujours des multiples entiers d'une même charge élémentaire.
Townsend obtint une valeur de 0.9*10-19 C pour les gouttes positives compatible avec la valeur de 1.0*10-19 C pour les gouttes négatives. Thomson refit l'expérience en 1901, et il obtint 1.1*10-19 C. En 1903, H.A. Wilson eut alors l'idée d'ajouter un champ électrique: en l'absence de champ, il mesurait ainsi la masse de chaque goutte par la vitesse limite, puis une vitesse limite différente en appliquant le champ (puisqu'une force électrique s'ajoutait au poids), ce qui lui permettait de calculer la charge électrique de la goutte. Il parvint à une charge élémentaire de 1.03*10-19 C. La valeur actuellement admise est un peu plus élevée, à 1.602*10-19. L'erreur vient problement de l'évaporation des gouttes pendant leur chute (ce qui réduit leur masse, et donc la charge calculée à partir du rapport q/m mesuré).
Millikan améliora cette mesure en remplaçant l'eau par l'huile, ce qui réduisait presque à zéro l'évaporation, et rendait par ailleurs l'expérience plus simple car il n'avait qu'une seule goutte d'huile à suivre au lieu des multiples gouttelettes d'un brouillard. De plus, Milikan laissait tomber chaque goutte en chute libre, puis la faisait remonter en appliquant un champ électrique, puis la laissait redescendre, répétant l'opération une dizaine de fois pour la même goutte. Il établit ainsi en 1911 un tableau des charges mesurées pour chacune des gouttes étudiées, de l'ordre de plusieurs dizaines de 10-19 C. La masse d'une goutte ne changeait pas d'une étape à l'autre, mais sa charge électrique changeait car elle acquerrait ou perdait des charges. Mais Millikan démontra que la variation de charge à chaque étape était (presque) toujours un multiple entier d'une unité qu'il évalua à 1.66*10-19 C.
On pouvait en déduire la masse de l'électron à partir du rapport q/m de Thomson. Millikan put également en déduire une valeur plus précise du nombre d'Avogadro (un faraday divisé par la charge de l'électron) à 6.06*1023 et donner ainsi une estimation de la masse l'atome d'hydrogène. On pouvait aussi en déduire la masse des atomes de chacun des éléments, et donc leur taille. Par exemple, la masse atomique de l'or étant de 197 (c'est-à-dire 197 grammes pour une mole d'or), la masse d'un atome d'or était de 0.197 kg/Nombre d'Avogadro, soit 3.25*10-25 kg. La densité de l'or étant de 19.3 kg/dm3, le diamètre d'un atome était voisin de 2.6*10-10 m. En fait les atomes de tous les éléments se révélèrent avoir des tailles de l'ordre de 10-10 m, longueur à laquelle fut attribué le nom d'Angström. L'existence réelle des atomes ne faisait plus de doute pour personne.
Il est ironique que Joseph John Thomson ait reçu le prix Nobel de physique en 1906 avoir démontré que l’électron était une particule, tandis que son fils George Paget Thomson reçut lui aussi le prix Nobel de physique en 1937 pour avoir démontré que l’électron était (aussi) une onde.
Tous des électrons!
Thosmon démontra en 1899 que les particules éjectées par les rayons ultraviolets dans l'effet photoélectrique avaient le même rapport masse/charge que les rayons cathodiques. Il s'agissait donc aussi d'électrons. Et les "ions" de Zeeman et Lorentz qui expliquaient en spectroscopie l'élargissement des raies proportionnellement au champ magnétique avaient le même rapport masse/charge (aux incertitudes de mesure près), et il s'agissait donc aussi d'électrons.
Et les rayons bêta découverts par Rutherford en 1898? Il s'agissait aussi d'électrons:
- Elster et Geitel n'observèrent pas de déviation en 1899
- Par contre Friedrich Giesel à Braunschweig (où il était chimiste dans une usine phamaceutique), Henri Becquerel à Paris, Stefan Meyer et Egon von Schweidler à l'université de Vienne en Autriche, observèrent la même année une faible déviation, dans la même direction que les rayons cathodiques
- Pierre et Marie Curie en 1900 établirent que la charge électrique des bêtas était négative, tandis que Becquerel et Dorn mesurèrent un rapport masse/ charge du même ordre de grandeur que les rayons cathodiques
- Kaufmann en 1902 mesura un rapport masse/charge identique (pour des bêtas de faible énergie, assez lents pour négliger les effets relativistes observés sur les bêtas de grande énergie)
- enfin, en 1948, Goldhaber et Goldhaber démontrèrent que les bêtas capturés par un atome ne se distinguaient absolument pas des électrons atomiques (sinon le principe de Pauli ne s'appliquerait pas à eux, ils pourraient occuper l'état d eplus basse énergie et émettre la différence d'énergie sous forme de rayons X, qui ne sont pas observés).
La Belle Époque
« Le monde a plus changé entre 1880 et 1914 que depuis les Romains (Charles Péguy)
L’Europe en 1890
La société de la « Belle Époque »
1% de a population possède 99% des richesses, et 99% de la population n'en possèdent que 1%
- Une aristocratie dont l’influence s’estompe

La comtesse Greffulhe en 1900
- Une grande bourgeoisie triomphante
- Une industrialisation qui s’accélère, surtout au Royaume-Uni, aux USA, en Allemagne, et en France
 Aciéries Carnegie (Ohio, 1910)
Aciéries Carnegie (Ohio, 1910)
- Une paysannerie en diminution
- 80% en Russie
- 55% en France et aux USA
- 40% en Allemagne
- 22% en Grande-Bretagne

- Un prolétariat en rapide augmentation
- Grèves très violentes
- Montée du socialisme
- Crispations du pouvoir
- Une petite bourgeoisie (employés, fonctionnaires) croissante
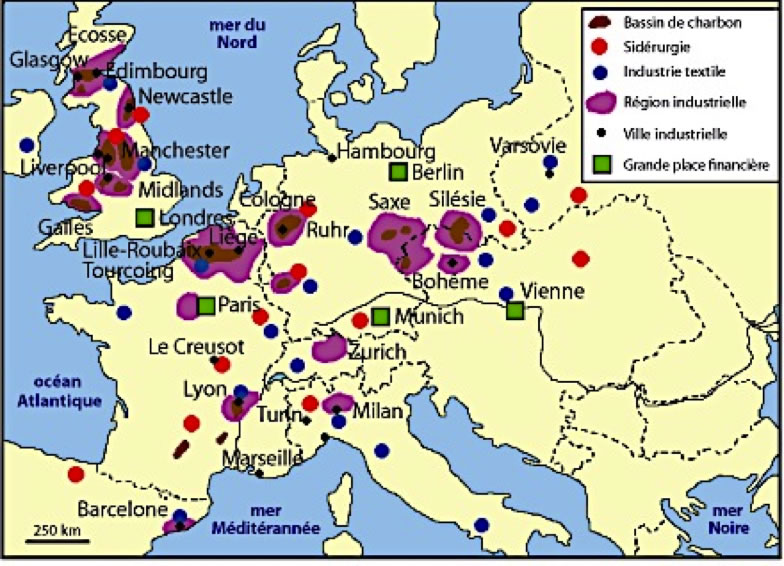
Carte de l’Europe industrielle vers 1900 © Audrey Longprés-Raillot
Âge du (de) fer
Architectures en fer
Le Crystal Palace de l’exposition de Londres (1851) 
- Viaduc de Garabit (Eiffel, 1884)

Principe du pont cantilever (Firth of Forth 1890) 
Navires, chemins de fer…
Canons…
Âge du charbon

 Abattage du charbon (France 1900)
Abattage du charbon (France 1900)
- Production (Grande-Bretagne)
- 1800: 5 millions de tonnes
- 1850: 50 millions de tonnes
- 1900: 240 millions de tonnes
- 1900: USA 350 Mt, Allemagne 125 Mt, France 40 Mt
Utilisations
- Vapeur
- Coke
- Chauffage
- Gaz de ville
 Eau et gaz à tous les étages !
Eau et gaz à tous les étages !


Égouts, eau courante… et WC
La Science triomphante
Biologie et médecine
Darwin (mais aussi Spencer et le « déclin de l’Occident » et le racisme « scientifique » )


Maladies contagieuses dues aux «germes» (bactéries, virus, parasites)
Asepsie, antisepsie, hygiène, vaccins => diminution rapide de la mortalité (surtout infantile)
Anesthésie => progrès en chirurgie
Pétrole
- Bitume
- Calfatage des bateaux en bois
- Routes (McAdam 1816)
- Pharmacie ???
- Éclairage
- Pétrole lampant (kérosène)
- Remplace l’huile de baleine


Panhard-Levassor (course Paris-Bordeaux 1895)
Production mondiale
- 1880: 30 M barils/an
- 1890: 77 Mb/an
- 1900: 149 Mb/an
- 1910: 328 Mb/an
Première raffinerie à Ploesti (Roumanie) en 1857
Moteurs à essence (de pétrole) Beau de Rochas (1862) – Otto (1867) – Daimler (1885) –Diesel (1893) 1891: Panhard-Levassor
La « fée électricité »
- Générateurs et moteurs à courant continu (Gramme 1870)

Dynamo de Z. Gramme (1870)
- Générateurs et moteurs à courant alternatif (Westinghouse 1886)
- Courant polyphasé (Tesla 1887)
- Locomotives électriques
- Métro de Londres (1890)
- Tramway de Zürich (1894)
- Ligne Berthoud-Thoune en Suisse (1899)
- Automobile
- Électroménager
- Fer à repasser électrique (1888)
- Cuisinière électrique (1893)
- Aspirateur (1906)
Éclairage électrique

Avenue de l’Opéra, à Paris, illuminée par des « bougies Jablochkoff » en 1878 alimentées par des dynamos Gramme
- Lampes à arc (Davy 1809)
- Ampoule à incandescence Swan (1878), Edison (1878)

- Lampe à arc Brush (1881)

Ampoule à incandescence d'Edison (1879)
Plus tard: lampes fluorescentes (E. Becquerel 1859, Hewitt 1901), lampes au néon (Claude 1910), lampes au sodium (1932)
Télécommunications
- Morse (1837)
- Très vite, réseaux télégraphiques continentaux
- Câbles sous-marins
- 1851: France-Angleterre
- 1853: Angleterre-Irlande
- 1858: Irlande-Canada
- 1871: Inde-Australie-Hong-Kong
- 1902: USA-Hawaii-Philippines
Socialement, l’ancêtre d’Internet
Équations de Maxwell ondes électromagnétiques Hertz (1887) Marconi (1895) : la TSF

Très brève sociologie des « savants »

- Image généralement positive * (quoique…)
- Le savant travaille presque toujours seul (avec un ou deux assistants cependant)
- Il s’agit très rarement d’une femme
- Il est souvent universitaire, ou professeur dans une école d’ingénieurs, et membre d’une institution savante (Royal Society, Académie des Sciences…)
 La Sorbonne en 1895
La Sorbonne en 1895
- Premier « gros » laboratoire: le Cavendish à Cambridge (1874)

Un laboratoire de pointe: J.J. Thomson au Laboratoire Cavendish de l’Université de Cambridge (vers 1900)
La physique en 1895
Des progrès considérables au cours du siècle
 William Thomson, Lord Kelvin (1824-1907)
William Thomson, Lord Kelvin (1824-1907)
- Mécanique, élasticité, résistance des matériaux Triomphe de la mécanique de Newton
- Astronomie (Laplace, Adams, Le Verrier )
- Mécanique du solide
- Mécanique des milieux continus (Young, Poisson…)
- Déformation des solides
- Plasticité, élasticité
- Compression, tension, cisaillement

- Physique des fluides
- Hydrodynamique
- Équations de Navier-Stokes
- Écoulements laminaires, turbulence

- Thermodynamique
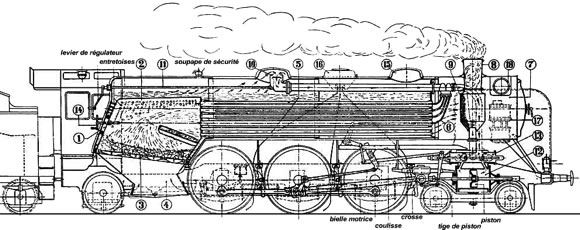
- Théorie de la chaleur
- Premier principe: conservation de l’énergie Mayer (1842), Joule (1843)
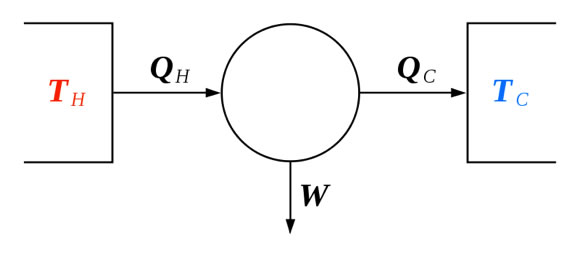
- Second principe: entropie croissante Carnot (1824), Clapeyron (1834), Clausius (1850), Kelvin (1851), Boltzmann (1873)
- Théorie statistique S = k Log W Maxwell (1866), Boltzmann (1872)
 Ludwig Boltzmann (1844-1906)
Ludwig Boltzmann (1844-1906)
- Électricité et magnétisme
- Ørsted (1820), Ampère (1820), Faraday (de 1830 à 1867)
- Maxwell
- Hertz
- Éther et tourbillons

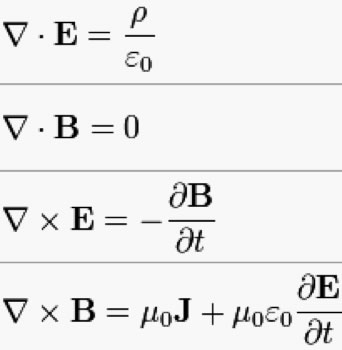
- Spectroscopie
- Joseph Fraunhofer (1787-1826)
 Raies du spectre solaire
Raies du spectre solaire
- Les raies sont caractéristiques de la nature chimique du corps qui les émet, de sa température et de sa vitesse
- Gustav Kirchhoff (1824-1887) et les 3 lois de la spectroscopie [Objet chaud = spectre continu, Gaz excité = spectre de raies , Objet froid = raies d’absorption]

Mais des domaines demeurent encore obscurs
- Les atomes existent-ils? Les chimistes en sont convaincus depuis le début du siècle (Proust, Dalton, Avogadro) pas les physiciens
- Émission et absorption de rayonnement par la matière (corps noir, effet photoélectrique, spectroscopie …)
- Nature des rayons cathodiques

« Fin de siècle »


Optimisme ou Pessimisme : Illustration d’Aubrey Beardsley pour la pièce Salomé d’Oscar Wilde (1893)